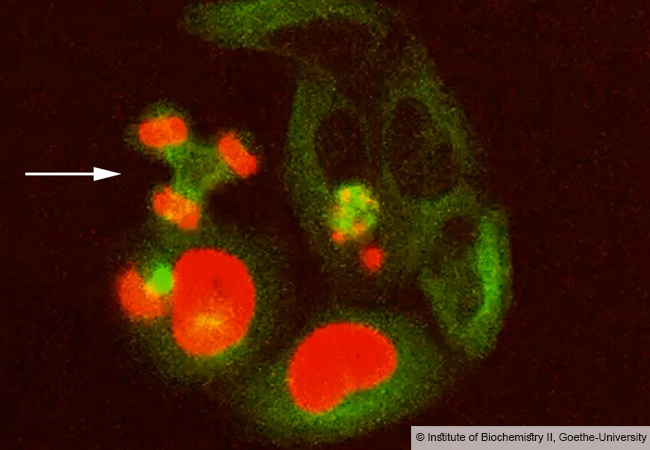
Wenn sich Krebszellen unkontrolliert teilen, spielen sogenannte Onkoproteine eine zentrale Rolle, die den Zellteilungszyklus managen. In normalen Zellen sind diese Proteine sehr kurzlebig und werden, da sich die Zellen gewöhnlich selten teilen, rasch wieder von der Zelle abgebaut. Das funktioniert in Krebszellen nicht mehr: Onkoproteine sind sehr langlebig, was zur unkontrollierten Zellvermehrung führt, und sie sind in aggressiven und therapieresistenten Krebsarten häufig zu finden. Solche Tumorarten werden auch als „Abbau-resistente Krebsarten“ (degradation resistant cancer) bezeichnet, gegen die weltweit mit Hochdruck nach wirksamen Therapien gesucht wird.
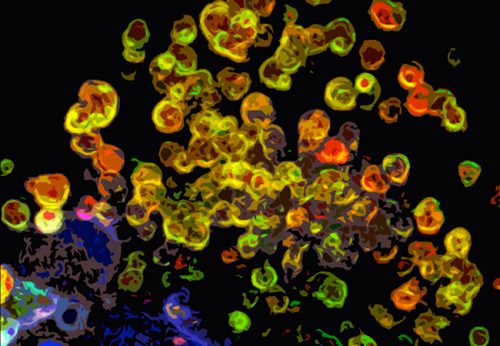
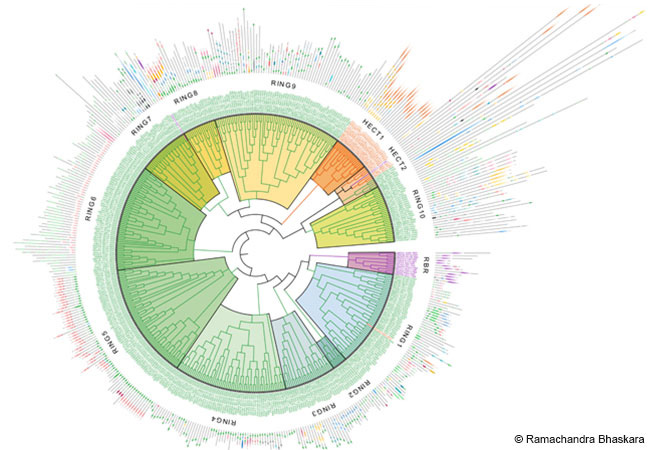
In einem gemeinsamen Forschungsprojekt untersuchen Wissenschaftler:innen des Technion – Israel Institute of Technology in Haifa, der Goethe-Universität Frankfurt und des Helmholtz-Zentrums München/Ludwig-Maximilians-Universität München solche Onkoproteine und versuchen, Ansatzpunkte für neue Therapien zu entwickeln. Das Projekt „Understanding and Targeting Degradation-resistant Cancers“ wird im Rahmen der Deutsch-Israelischen Projektkooperation (DIP) mit 1,6 Millionen Euro gefördert. Die DIP wurde 1997 vom Bundesministerium für Bildung und Forschung (BMBF) ins Leben gerufen, um die Exzellenz in der deutsch-israelischen Forschungszusammenarbeit zu stärken. Die Deutsche Forschungsgemeinschaft (DFG) hat das Programm übernommen und führt es fort, während das BMBF weiterhin die fünfjährigen Projekte finanziert.
An dem Projekt sind drei Wissenschaftler von Technion beteiligt, Ashraf Brik, Amir Orian and Dan Bracha, auf deutscher Seite forschen Gruppen in Frankfurt und München unter der Leitung von Prof. Ivan Đikić vom Institut für Biochemie II der Goethe-Universität und Markus E. Diefenbacher, Professor an der Ludwig-Maximilians-Universität München und Gruppenleiter am Helmholtz Zentrum München. Das Ziel: Die Wissenschaftler:innen wollen die grundlegenden molekularen Mechanismen entschlüsseln, die für die Stabilisierung der Onkoproteine verantwortlich sind, und daraus Ansatzpunkte für neue Therapien entwickeln. Dazu wollen sie Zielstrukturen für klassische Wirkstoffe (sogenannte small molecules) identifizieren sowie Wirkstoffe finden, die den Abbau der Onkoproteine beschleunigen, sogenannte PROTACs (Proteolysis Targeting Chimeric Molecules). Mithilfe von PROTACs sollen die Onkoproteine mit der zellulären Markierung Ubiquitin versehen und so dem zellulären Recyclingsystem zugeführt werden.
Eine zentrale Rolle im Projekt nimmt das Frankfurt Competence Center for Emerging Therapeutics (FCET) ein, das kürzlich als Teil des Goethe-Zentrums für (Hoch-)Technologie (Go4Tec) gegründet wurde. Als Innovationszentrum bietet das FCET Zugang zu High-End-Instrumenten und -technologien.