Der Ablauf der Lebenszeit fast aller Organismen gehorcht mathematisch beschreibbaren Regeln. Dementsprechend erwartet man eine biologische Uhr, die Ablauf und Ende des Lebens steuert. Wie könnte man ihr »Ticken« feststellen? Und warum hört es irgendwann auf?
Seit der Antike symbolisieren die Menschen den Ablauf der Lebenszeit mit einer Sanduhr. Gleichzeitig messen sie die Zeit in Einheiten von Sekunden, Tagen und Jahren, indem sie sich an periodischen Vorgängen orientieren. Ursprünglich waren dies astronomische Perioden (der Erdumlauf um die Sonne, die Eigendrehung der Erde etc.). Heute sind es atomare Schwingungen. Atomuhren haben inzwischen einen Gangfehler von einer Sekunde in 30 Millionen Jahren erreicht.
 Aber sind diese Dimensionen – so sehr sie uns selbstverständlich geworden sind – überhaupt dazu geeignet, biologische Zeiten zu messen? Das Leben von Organismen unterteilt sich in die Zeitabschnitte der Embryogenese (Keimesentwicklung), Ontogenese (Wachstum), Alterung (Seneszenz) und Tod. Ihre physikalische Dauer ist sehr variabel.
Aber sind diese Dimensionen – so sehr sie uns selbstverständlich geworden sind – überhaupt dazu geeignet, biologische Zeiten zu messen? Das Leben von Organismen unterteilt sich in die Zeitabschnitte der Embryogenese (Keimesentwicklung), Ontogenese (Wachstum), Alterung (Seneszenz) und Tod. Ihre physikalische Dauer ist sehr variabel.
So kann die Embryonalentwicklung bei Tieren je nach Umgebungstemperatur selbst bei der gleichen Art sehr unterschiedlich lange dauern oder die Seneszenz ausbleiben. Dennoch sind für diese Zeitabschnitte von der Natur klare Zeitrahmen vorgegeben. Wie sehen ihre möglichen Taktgeber aus?
Man muss nicht lange suchen, um in tierischen Organismen sich regelmäßig wiederholende Vorgänge zu finden, die als biologische Uhren geeignet wären. Jeder kennt den »Augenblick«, einen »Atemzug« oder einen »Herzschlag« als Zeitangabe. Interessant ist, dass die periodischen Vorgänge untereinander gekoppelt sind:
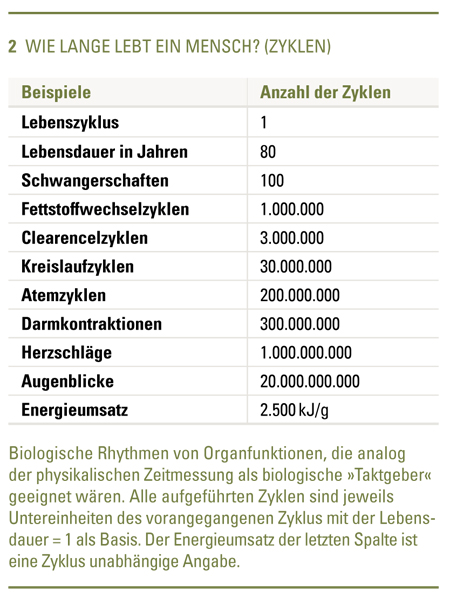
Auf vier Herzschläge kommt etwa ein Atemzug; auf einen Atemzug rund hundert Augenblicke. Und so lässt sich die Lebenszeit nicht nur in Jahren, sondern auch in biologischen Rhythmen oder Zyklen angeben. Zumindest bei den Säugetieren ist die Summe dieser Zyklen innerhalb der natürlichen Lebensdauer sehr konstant. (Abb. 2) Doch warum lebt eine Maus nur drei bis vier Jahre, während ein Wal bis zu 100 Jahre alt werden kann?
Schwere leben länger
Offenbar hat das Körpergewicht einen natürlichen Einfluss auf die Lebensdauer. Zwischen beiden Größen herrscht eine einfache Korrelation: Je schwerer (größer) ein Organismus ist, desto höher ist seine Lebenserwartung. Diese Beziehung lässt sich mit einer einfachen mathematischen Gleichung beschreiben, die für alle Tiere gilt: Lebensalter (A) = a · Masse (M)0.25 Daran lässt sich ablesen, dass man eine Verdopplung der Lebenszeit erhält, wenn die Masse um den Faktor 16 zunimmt. (Der Exponent 0.25 steht für die vierte Wurzel aus der Masse; a ist eine Konstante.)
Es gibt nur ein Tier, das völlig aus der Rolle fällt. Es ist der Nacktmull. (Abb. 3) Wir haben 108 biologische Rhythmen wie Atem- und Kreislaufzyklen, Darmkontraktionen oder Herzschläge in Relation zum Gewicht des jeweiligen Organismus gesetzt. Der sich ergebene Korrelationsexponent von 0.248 ± 0.054 – zeigt eine praktisch identische Übereinstimmung mit der Korrelation zwischen Gewicht und Lebensspanne. Demnach hört unsere biologische Uhr auf zu ticken, wenn eine bestimmte Zahl von Zyklen durchlaufen ist. Doch wie wird diese Zahl festgelegt? Darauf geben verschiedene Alternstheorien unterschiedliche Antworten.
Japaner und ihre Autos leben länger!
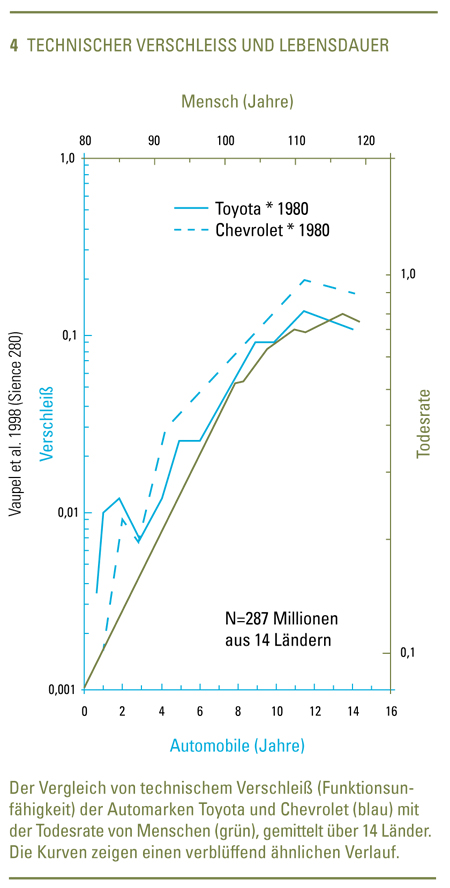
Eine verbreitete Ansicht ist, dass unsere Lebensspanne durch den Verschleiß des Organismus begrenzt wird. Unstrittig ist, dass Organfunktionen im Verlauf des Lebens einen zum Teil dramatischen Leistungsverlust erleiden, der lebensverkürzend wirkt. So erreichen die Lunge und die Nieren von 70- bis 75-Jährigen nur noch 50 Prozent der Leistung eines Jugendlichen von 18 bis 20 Jahren.
In der renommierten Fachzeitschrift Science gingen Vertreter der Verschleißtheorie soweit, die Lebensspanne von Menschen mit der Haltbarkeit verschiedener Automarken zu vergleichen. (Abb. 4) Sie wiesen auch darauf hin, dass die Japaner – wie ihre Autos – weltweit am längsten leben. Es ist schon erstaunlich, wie undifferenziert Autoren solche Analogien postulieren. Auch die Theorie der freien Radikale gehört zu den Verschleißtheorien.
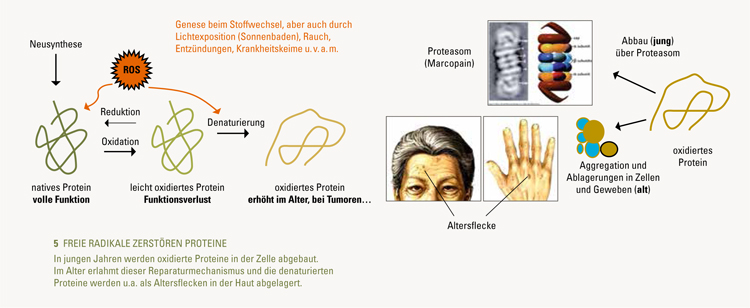
Freie Radikale sind kurzlebige, sehr reaktionsfreudige Verbindungen, die den Körper durch Oxidationen schädigen können. (Abb. 5) Die meisten freien Radikale entstehen in Mitochondrien, den Kraftwerken der Zelle, bei normalen Stoffwechselvorgängen. Aber sie können auch durch äußere Einflüsse wie UV-Strahlung oder gefährliche Umweltgifte entstehen. Von besonderer Bedeutung für Alternsprozesse sind Radikale von Sauerstoff-Verbindungen (ROS).
Dazu gehören Stoffe wie Ozon oder Wasserstoffperoxid. Ihren schädlichen Wirkungen versucht man mit Antioxidantien entgegenzuwirken. Diese finden sich v. a. in Früchten, Gemüse, Reis, Ölen, Tee, Kaffee und Kakao sowie in der menschlichen Muttermilch. Wie wirksam der Verzehr von Antioxidantien ist, bleibt fraglich, zumal Radikale auch nützliche Funktionen im Körper erfüllen, etwa bei der Bekämpfung von Viren und Bakterien.
Ein Gen für die Unsterblichkeit?
Mittlerweile führt man die Begrenzung der Lebensdauer weniger auf Verschleiß zurück als vielmehr auf ein genetisches Programm. Es sind inzwischen über 200 Gene entdeckt worden, die ins Alternsgeschehen involviert sind. An unserer Universität erforscht insbesondere Prof. Heinz Osiewacz am Fachbereich Biowissenschaften die molekularen Grundlagen dieser Erbfaktoren. Beim Pilz Podospora anserina fand er diverse Gen-Mutationen sowohl im Kern als auch in den Mitochondrien, die vor allem in die Atmungskette eingreifen.
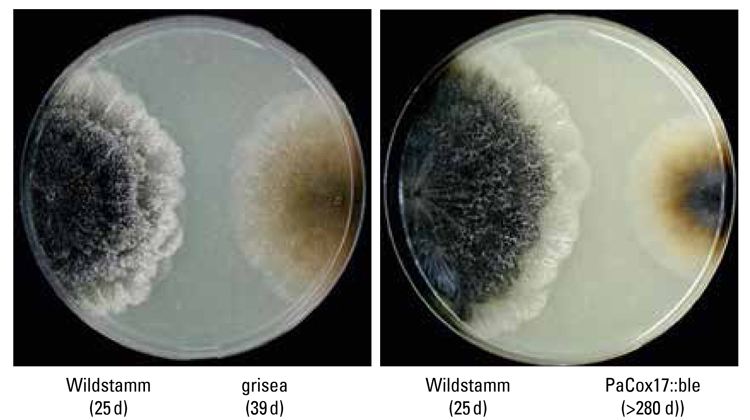
Einige bewirken, dass die natürliche Lebensdauer des Wildstamms von rund 25 Tagen zum Teil vervielfacht wird, ja, dass Pilze sogar unsterblich werden, zum Beispiel die Mutanten ex1, mex1 und zahlreiche andere. (Abb. 6) Gene, die das Altern und damit die Lebenserwartung z. T. dramatisch verändern, fand man bei vielen Organismen – auch beim Menschen.
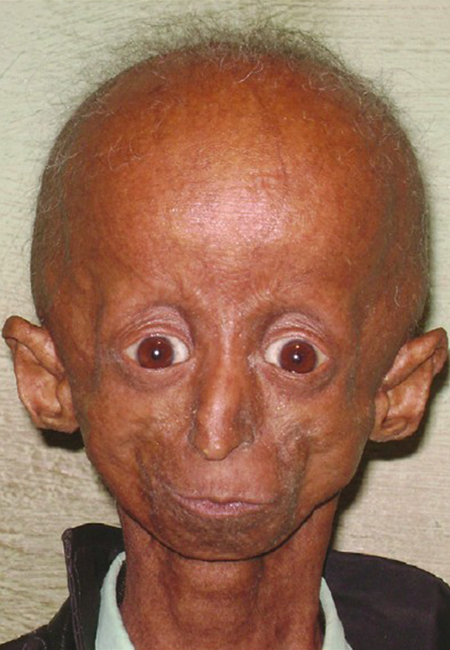
Deutlich verkürzt ist die Lebenserwartung beim Hutchinson-Gilford-Syndrom, auch Progeria infantilis genannt. Sie liegt bei durchschnittlich 14 Jahren. Bereits in der Kindheit zeigen die Betroffenen deutliche Spuren des Alterns. (Abb. 7) Bei der Form Progeria adultorum (Werner-Syndrom) tritt beschleunigtes Altern bei Erwachsenen etwa ab der Lebensmitte auf.
Sex = Ex!?
Auch die Beobachtung, dass viele Pflanzen und Tiere ohne erkennbare Alterung kurz nach erfolgreicher Fortpflanzung sterben, spricht dafür, dass die Lebenszeitbegrenzung genetisch festgelegt ist. Dieser »programmierte Tod« (auf Zellniveau »Apoptose« genannt) geht so weit, dass viele Insekten als erwachsene, geschlechtsreife Organismen keine Verdauungsorgane mehr haben.
Der Sinn ihres letzten Lebensstadiums dient allein der Weitergabe ihrer Gene. Das bekannteste Beispiel ist die Eintagsfliege, die nur einen Tag zum Zwecke der Fortpflanzung lebt. Auch Verwandte der Säugetiere zeigen diese Eigenschaft: Männchen der Breitfuß-Beutelmäuse sterben kurz nach erfolgreicher Paarung im Alter von maximal elf bis zwölf Monaten. Weibchen können dagegen über drei Jahre alt werden.
Post-Doktorand gegen Nobelpreisträger: Die Hayflick-Grenze
Auch die Entdeckung des amerikanischen Gerontologen Leonhard Hayflick spricht dafür, dass die Lebensspanne genetisch festgelegt ist. Er widerlegte als Post-Doktorand die Behauptung des französischen Nobelpreisträgers Alexis Carrel, dass sich Zellen von Wirbeltieren in Kultur unbegrenzt teilen können und damit unsterblich sind. Carrel, ein Chirurg und Biologe, hatte u.a. Zellen von Kükenherzen kultiviert.
 Als sie nach 24 Jahren noch immer schlugen, obwohl Hühner nur sieben bis zehn Jahre leben, folgerte er 1908: »Man kann sagen, daß die Zellen unsterblich sind.« Hayflick konnte allerdings 1961 zeigen, dass Carrel mit der Nährlösung immer wieder junge, noch teilungsfähige Zellen in die Kultur gebracht hatte. Er schloss dies durch eine veränderte Versuchsanordnung aus und fand heraus, dass alle Zellen nur zu einer begrenzten Anzahl von Zellteilungen fähig sind, bevor der programmierte Zelltod (Apoptose) eintritt.
Als sie nach 24 Jahren noch immer schlugen, obwohl Hühner nur sieben bis zehn Jahre leben, folgerte er 1908: »Man kann sagen, daß die Zellen unsterblich sind.« Hayflick konnte allerdings 1961 zeigen, dass Carrel mit der Nährlösung immer wieder junge, noch teilungsfähige Zellen in die Kultur gebracht hatte. Er schloss dies durch eine veränderte Versuchsanordnung aus und fand heraus, dass alle Zellen nur zu einer begrenzten Anzahl von Zellteilungen fähig sind, bevor der programmierte Zelltod (Apoptose) eintritt.
Die Zahl an natürlichen Teilungen (Hayflick-Zahl) variiert dabei von Spezies zu Spezies. Beim Menschen sind es rund 50. Nur die Teilungsfähigkeit der Stammzellen unterliegt nicht der Hayflick- Grenze. Dies gilt auch für entdifferenzierte Tumorzellen. Deshalb können sie sich unkontrolliert teilen und vermehren.
Lebe langsam, lebe länger!?
Da nun vieles dafür spricht, dass ein genetisches Programm festlegt, wie lange unsere biologische Uhr tickt, bis der Sand durch das Stundenglas unseres Lebens gerieselt ist, stellt sich die Frage, ob wir überhaupt einen Einfluss auf unsere Lebensspanne haben. Tatsächlich gibt es einen erstaunlichen Zusammenhang zwischen der Stoffwechselrate und der Größe eines Organismus, die wiederum die Lebensdauer beeinflusst:
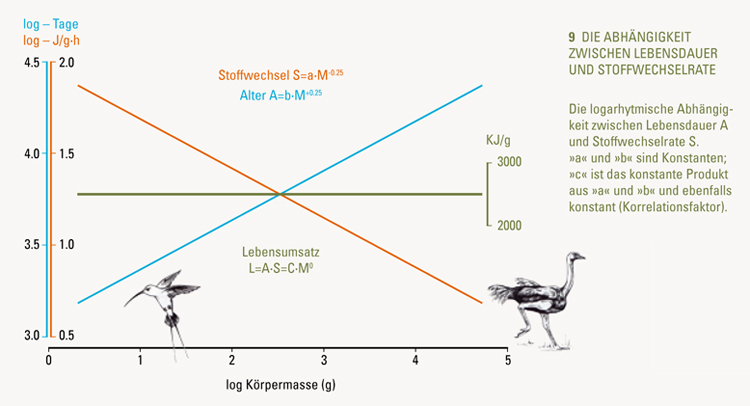
Je größer und schwerer ein Organismus ist, umso niedriger ist seine spezifische Umsatzrate, gemessen in Joule pro Gramm und Stunde (J/g·h; Abb. 9) Der Korrelationsexponent für die Beziehung zwischen der Masse und der Stoffwechselrate beträgt – 0.25. Das bedeutet, dass eine Erhöhung der Masse M um den Faktor 16 die Stoffwechselwrate S halbiert.
[dt_call_to_action content_size=“small“ background=“fancy“ line=“false“ animation=“none“]
Auf den Punkt gebracht
- Unsere Lebenszeit ist durch eine bestimmte Zahl an biologischen Rhythmen und Zyklen wie Atmung und Herzschlag festgelegt.
- Die Lebensuhr »tickt« in Stoffwechseleinheiten. Am längsten leben Organismen mit einer großen Körpermasse und niedriger Stoffwechselrate wie Schildkröten oder Wale.
- Vieles spricht dafür, dass die Lebensspanne genetisch festgelegt ist. Verschleiß spielt die primäre Rolle.
[/dt_call_to_action]
(Abb. 8) Spannend wird es nun, wenn wir beide Korrelationen zusammenbringen und damit die Frage beantworten, wie viel ein Organismus im Laufe seines Lebens an Energie umsetzt (L). Dazu muss man das Produkt aus der Lebensdauer und der Stoffwechselrate bilden: L = A · S = a ·b ·(M^-0.25 · M^+0.25) = a · b · M^0 = c (konstant)
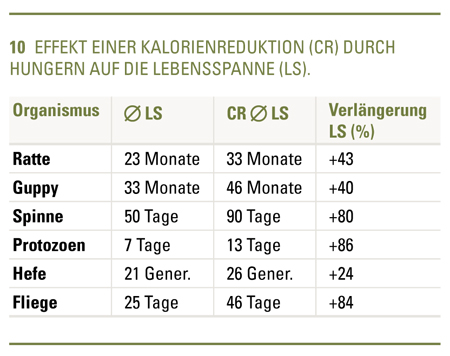 Das bedeutet, dass unabhängig von Masse und erreichbarem Alter der Lebensumsatz ein konstanter Wert ist, die Lebensuhr also in Stoffwechseleinheiten abläuft. Daraus folgt aber zwingend, dass eine Reduktion der Stoffwechselrate zu einer Verlängerung der Lebenszeit führt, da die Uhr in diesem Fall langsamer abläuft. (Abb. 10) Diese Stoffwechseltheorie ist experimentell leicht zu überprüfen.
Das bedeutet, dass unabhängig von Masse und erreichbarem Alter der Lebensumsatz ein konstanter Wert ist, die Lebensuhr also in Stoffwechseleinheiten abläuft. Daraus folgt aber zwingend, dass eine Reduktion der Stoffwechselrate zu einer Verlängerung der Lebenszeit führt, da die Uhr in diesem Fall langsamer abläuft. (Abb. 10) Diese Stoffwechseltheorie ist experimentell leicht zu überprüfen.
Wir haben sie in unserem Institut vielfach bestätigen können. Sie hat sogar für einzelne Lebensabschnitte Gültigkeit. So beträgt der Energieumsatz bei Vögeln in der Embryogenese 2 kJ/g, in der Jugendentwicklung 20 kJ/g und in der Adultphase insgesamt 2 500 kJ/g. Tiere mit niedriger Stoffwechselrate (z. B. Schildkröten), die Energiesparphasen im Lebensablauf haben (z. B. Winterschläfer) oder die man hungern lässt, leben um die Zeitspanne länger, die sie durch den reduzierten Stoffwechsel gewonnen haben.

Wir sehen, dass es nicht einen allein bestimmenden »Taktgeber« gibt, sondern dass zahlreiche, sehr variable Zahnräder der Lebensuhr ineinandergreifen, die gemeinsam den zeitlichen Ablauf des Lebens beeinflussen. Sie gewährleisten so eine hohe Flexibilität der Organismen. Und vieles spricht dafür, dass Gene die Grundlage dafür festlegen, wie lange unsere biologische Uhr tickt. Ein sehr wichtiger Aspekt ist allerdings der Stoffwechsel, die ultimative Grundlage jeden Lebens. Halten wir ihn reduziert – will heißen: weniger (und gesünder) essen und gelassener leben, können wir unsere Lebensspanne ein wenig verlängern.
[Autor: Prof. Dr. Roland Prinzinger]