Im November besuchen die US-Wissenschaftler Dr. Erica und Prof. Dr. Justin Sonnenburg die Goethe-Universität im Rahmen der Friedrich-Merz-Stiftungsgastprofessur. Ihr Forschungsschwerpunkt sind kleine Organismen mit großem Einfluss auf unser Leben und unsere Gesundheit.
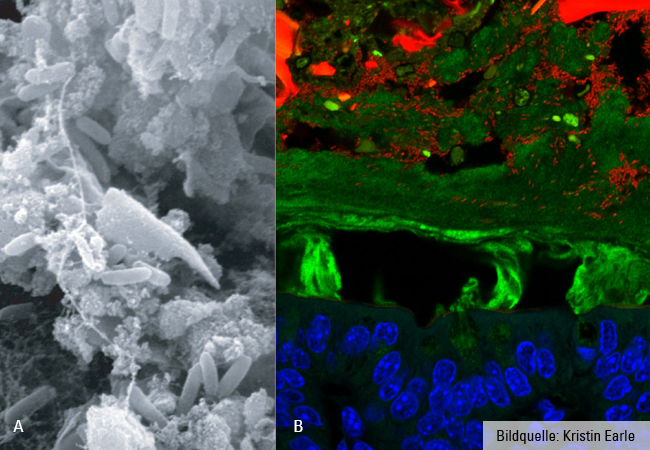
Bild A: B. theta eingebettet in Schleim sowie Nahrungspartikel. Bildquelle: Jamie Dant und Justin Sonnenburg
Bild B: B. theta im Darm umherwandernd. B. theta: die kleinen roten Stäbchen; das Grüne: Schleim, das Blaue: Wirtsepithel/Kolonozyten. Bildquelle: Kristin Earle
Darmmikrobiom, so wird die Gesamtheit der in unserem Darm lebenden Mikroorganismen genannt. 10 bis 100 Billionen von ihnen tummeln sich dort – Viren, Archaeen und Pilze, aber vor allem Bakterien. Wir Menschen leben in einer Symbiose mit diesem Sammelsurium winzig kleiner Darmbewohner, die ein Ökosystem bilden und zusammen, als Gemeinschaft, wertvolle Dienste für den Menschen verrichten. Es hilft, unser Immunsystem fit zu halten. Zudem ist es am Stoffwechsel beteiligt. Und es „redet“ sogar mit unserem Gehirn. Über bestimmte Kommunikationskanäle tauschen beide Informationen aus. Das Darmmikrobiom könnte dadurch auch Einfluss auf unsere Psyche haben.
Erica und Justin Sonnenburg von der kalifornischen Stanford University erforschen seit vielen Jahren, wie genau der Symbiosepartner des Menschen funktioniert, welche Erkrankungen durch eine Dysbiose, ein aus der Balance geratenes Darmmikrobiom, entstehen und wie sich diese in Zukunft in Form von neuen Therapien oder Medikamenten behandeln lassen könnten. Im Speziellen geht das US-Forscherpaar der Frage nach, wie sich unsere Ernährung auf das Verhalten der Darmmikroben auswirkt und wie dies wiederum unsere Gesundheit beeinflusst. Denn: Was wir essen, ernährt nicht nur uns – sondern auch die Darmmikroben.
Eines ihrer Forschungsobjekte sind daher MACs. MAC steht für microbiota-accessible carbohydrates, also Kohlenhydrate, die für das Mikrobiom zugänglich sind. Sie sind das Futter der Darmmikroben. Der Stoff, der sie gedeihen lässt. „Die Genome der in unserem Darm lebenden Bakterien, die übrigens über 99 Prozent unseres genetischen Materials ausmachen, sind sehr gut darin, komplexe Kohlenhydrate aus pflanzlicher Nahrung abzubauen“, erklärt Erica Sonnenburg. „Sie verzehren die MACs und produzieren als Ergebnis ihres Stoffwechsels viele Arten kleiner Moleküle. Von denen gehen einige in den Blutkreislauf über und können in unserem gesamten Körper zirkulieren.“
Ballaststoffreich und fermentiert
Wer seinem Darmmikriobiom etwas Gutes tun will, muss also Lebensmittel essen, die viele MACs enthalten. Dazu gehört Ballaststoffreiches wie Bohnen, Hülsenfrüchte, Gemüse, Obst, Vollkornprodukte, Nüsse und Samen. Mindestens 50 Gramm oder mehr Ballaststoffe sollten wir pro Tag zu uns nehmen, rät Erica Sonnenburg. Eine Wohltat für das Mikrobiom sind auch fermentierte Lebensmittel: Joghurt, Kefir, Sauerkraut, Kimchi, also eingelegter koreanischer Kohl, oder Kombucha, ein fermentierter asiatischer Tee.
Das Problem ist nur, dass die Ernährung bei vielen Menschen in modernen Gesellschaften anders aussieht, ballaststoffarm und unfermentiert. Auf ihrem Speiseplan stehen allzu oft industriell stark verarbeitete Lebensmittel: Tiefkühlpizza, süße und salzige Snacks, Kekse, Geflügelnuggets oder Instant-suppen. Die enthalten viel Zucker, Fett und Salz, auch Emulgatoren, künstliche Süßstoffe oder andere Produkte der modernen Lebensmittelindustrie. Damit kann das Darmmikrobiom nichts anfangen. „Es ist dann gezwungen, sich auf die einzige andere Nahrungsquelle zu stürzen, die sich anbietet – und das ist die Schleimhaut des Darms. Wenn wir also keine Pflanzen essen, beginnt das Mikrobiom, uns zu essen.“ Das Immunsystem reagiert darauf und löst Alarm in Form von Entzündungen aus. Es versucht so zu verhindern, dass die Darmmikroben dem menschlichen Gewebe, das den Darm auskleidet, zu nahekommen und sich daran gütlich tun. „Da läuft eine richtige Entzündungskaskade ab. Wir vermuten, dass diese an der Entstehung von chronischen Krankheiten wie Herz-Kreislauf-Erkrankungen und Autoimmunerkrankungen wie Morbus Crohn wesentlich beteiligt ist. Auch an der Entstehung einiger Krebsarten, bei denen Entzündungen die Hauptrolle spielen.“
Ein schlecht aufgestelltes Darmmikrobiom kann aber noch auf andere Art Ungemach bringen. Hier geht es ums tadellose Funktionieren unseres Immunsystems. Dieses hat ja die Aufgabe, Angreifer zu erkennen und abzuwehren – die Immunreaktion. „Dafür muss es echte Bedrohungen wie einen eindringenden Infektionserreger von etwas Harmlosem wie der aufgenommenen Nahrung unterscheiden können“, so Justin Sonnenburg. Das Darmmikrobiom hilft dabei. Es trainiert das Immunsystrem darauf, Freund und Feind fein säuberlich auseinanderzuhalten. Dafür sind beide, Immunsystem und Darmmikroben, permanent in eine Art Gespräch vertieft. Sie tauschen Informationen aus. Gerät diese „Konversation“ ins Stocken, hat das weitreichende Folgen: „Das Immunsystem beginnt dann plötzlich Fehler zu machen. Es hält etwas komplett Ungefährliches, eine Erdnuss oder gar körpereigene Zellen, für gefährlich.“ Auch diese möglicherweise auf ein beschädigtes Darmmikrobiom zurückgehende Fehleinschätzung kann uns krank machen und zur Entwicklung von Autoimmunkrankheiten oder einer Reihe anderer chronischer Erkrankungen führen.
Grund genug, die Darmmikroben mit reichlich MACs zu versorgen. Wer sich länger ungesund ernährt hat und deswegen schon unter Entzündungen leidet, für den ist es aber nicht zu spät. „Wir haben entdeckt, dass Ernährungsumstellungen viel Positives bewirken können“, sagt Erica Sonnenburg. „Fermentierte Lebensmittel wie Joghurt und Sauerkraut sind ein wirklich wirksames Mittel, um Entzündungen, die schon aufgetreten sind, zumindest wieder abzuschwächen.“ Und damit nicht genug: Mit verändertem Speiseplan lässt sich auch die Vielfalt in einem geschädigten Mikrobiom wieder erhöhen – ein ganz entscheidender gesundheitlicher Aspekt. Denn je mehr unterschiedliche Mikroben im Darm leben, desto besser können sie als Ganzes ihre Aufgaben erfüllen. Und je weniger es sind, desto eher werden wir krank. Zum Beispiel besteht ein Zusammenhang zwischen einer reduzierten Mikrobenvielfalt und Adipositas oder Typ-2-Diabetes.
Verarmtes Darmmikrobiom
Auch in punkto Mikrobenvielfalt hängt wieder vieles an der Ernährung. Wobei nicht nur industriell verarbeitete Lebensmittel schlecht dafür sind, sondern auch die Einnahme von Antibiotika und – ganz am Anfang des Lebens – industriell gefertigte Säuglingsnahrung. Weswegen Menschen in industriellen Gesellschaften nur ein paar Hundert unterschiedliche Mikrobenarten aufweisen. „Solch ein Darmmikrobiom erscheint geradezu verarmt, wenn wir es mit dem von nicht industrialisierten Jäger- und Sammlervölkern vergleichen, die wegen ihrer Ernährung über eintausend unterschiedliche Arten von Mikroben im Darm haben.“
Wie lässt sich die Erforschung des Zusammenspiels der Darmmikroben grundsätzlich einordnen? „Jeder weiß, dass Organe wie Herz und Leber lebenswichtig sind“, antwortet Justin Sonnenburg. „Aber auch das Darmmikrobiom gehört in diese Kategorie, weil es enormen Einfluss auf unsere Gesundheit und unser Wohlbefinden ausübt.“ Wie die wissenschaftlichen Ziele für die nächsten Jahre aussehen? „Wir wollen noch genauer verstehen, wie das Darmmikrobiom vom Säuglings- bis zum Erwachsenenalter funktioniert – und dieses Wissen dann nutzen, um bessere Strategien und Behandlungen zur Vorbeugung und Heilung von Krankheiten zu entwickeln. Dabei haben wir die kleinen Moleküle, die vom Mikrobiom produziert werden, im Blick. Einige von ihnen könnten die Grundlage für künftige Arzneimittel zur Behandlung einer Reihe von nicht übertragbaren, chronischen Krankheiten bilden.“ Diese Medikamente zu entwickeln, dauert viele Jahre. Schneller ließe sich das Darmmikrobiom – und damit unsere Gesundheit – durch eine Ernährungsumstellung stärken. „Damit kann jeder Mensch sofort anfangen.“
Im November besuchen die Sonnenburgs Frankfurt im Rahmen der Friedrich-Merz-Stiftungsgastprofessur. Sie nehmen an einem wissenschaftlichen Kongress an der Goethe-Universität teil, zudem gibt es eine öffentliche Bürgerveranstaltung. Dabei wird der Film „Unser Bauch. Die wunderbare Welt des Mikrobioms“ vorgeführt, an dem die beiden als Experten mitgewirkt haben. Bei ihrem Besuch wollen sie mit vielen Leuten reden, nicht nur mit anderen Mikrobiom-Forschern. Ihre Arbeit sei immer schon auch durch den Austausch mit Ernährungswissenschaftlern, Ärzten und Ingenieuren angeregt worden. Die Sonnenburgs freuen sich darauf, mehr über die „großartige Arbeit“ an der Goethe-Universität zu erfahren. Und sie möchten die Gelegenheit nutzen, ihr Wissen über das Darmmikrobiom auch an die Einwohner Frankfurts weiterzugeben.
Andreas Lorenz-Meyer
1
Die Friedrich-Merz-Stiftungsgastprofessur wurde im Dezember 1985 anlässlich des 100. Geburtstags von Firmengründer Friedrich Merz gestiftet, der als einer der ersten Mitglieder der Senckenbergischen Gesellschaft mit der Frankfurter Universität eng verbunden war und die Wissenschaft gefördert hat. Ziel der Stiftungsgastprofessur ist, einen besonders angesehenen Wissenschaftler aus den Bereichen Pharmazie oder Humanmedizin an die Goethe-Universität Frankfurt zu berufen. 1987 zum ersten Mal verliehen, wurde die Gastprofessur bis auf zwei Ausnahmen jährlich vergeben. Die Gastprofessur und das Symposium, dessen Themenspektrum von der Grundlagen- bis zur Versorgungsforschung reicht, bieten Forschern aus Hochschule und Industrie jährlich die Gelegenheit zum Wissensaustausch und zu einer weitergehenden Zusammenarbeit. Mehr Infos zu den Terminen der diesjährigen Gastprofessur auf S. 27 des UniReport.
2
Friedrich-Merz-Stiftungsgastprofessur 2024
Dietary and therapeutic microbiome modulation: State of the art and perspectives
Kuratorin: Prof. Dr. med. Maria J. G. T. Vehreschild, Leiterin Schwerpunkt Infektiologie, Medizinische Klinik II, Universitätsklinikum Frankfurt.
12. November 2024
Students Lecture am Uniklinikum
10 bis 12 Uhr, Universitätsklinikum Frankfurt.
Das Ehepaar Sonnenburg hält einen Vortrag zum Thema: »Industrialization of the Gut Microbiome and the Rise of Chronic Inflammatory Disease« für Studierende und Interessierte mitanschließender Fragerunde.
13. November 2024
Wissenschaftliches Symposium: Dietary and therapeutic Microbiome Modulation – State of the Art and Perspectives.
9 bis 17 Uhr, Universitätsklinikum Frankfurt, Gebäude 6.
14. November 2024
Unser Bauch. Die wunderbare Welt des Mikrobioms
18 bis 20 Uhr, Kino Orfeos Erben, Hamburger Allee 45, Frankfurt am Main.
(ARTE France, 2019). Filmgespräch mit Prof. Dr. Justin und Dr. Erica Sonnenburg (Stanford University/USA) und Prof. Dr. med. Maria J.G.T. Vehreschild (Goethe-Universität).
Mehr Informationen und zur Anmeldung unter
https://www.uni-frankfurt.de/Friedrich-Merz-Stiftungsgastprofessur