Ein Forschungsteam um Beate Averhoff und Volker Müller von der Goethe-Universität Frankfurt hat einen fundamentalen Mechanismus entdeckt, der dem gefürchteten Krankenhauskeim Acinetobacter baumannii beim Überleben hilft. Dieser Mechanismus macht deutlich, warum der Keim in Krankenhäusern schwer auszurotten ist und Infektionen in Patienten immer wieder aufflammen: Wenn die Lebensbedingungen für die Bakterien zu ungünstig werden, fallen sie in eine Art Dornröschenschlaf. Dann können sie mit gängigen diagnostischen Standards nicht mehr entdeckt und auch nicht mehr abgetötet werden. Aus diesem „tiefen Schlaf“ erwachen sie, wenn sich die Lebensbedingungen wieder besser werden.
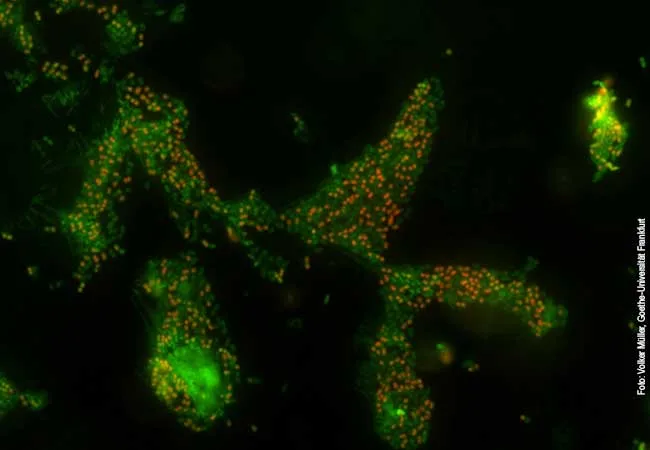
Das Bakterium Acinetobacter baumannii ist ein äußerst gefährlicher Erreger im Krankenhaus: Viele der Bakterienstämme sind gegen Antibiotika aus unterschiedlichen Stoffklassen resistent. Infektionen mit Acinetobacter baumannii wurden erst während des Irak-Krieges vermehrt beobachtet und nehmen seitdem mit rasantem Tempo weltweit zu. Daher hat die Weltgesundheitsorganisation WHO Acinetobacter baumannii auf Platz eins der Liste der Bakterien gesetzt, gegen die dringend neue Medikamente benötigt werden. Die gefährliche Verbreitung von Acinetobacter baumannii geht aber nicht nur die Antibiotikaresistenzen zurück, sondern auch auf seine enorme Anpassungsfähigkeit: Er wächst auch unter harschen Bedingungen wie Trocken- und Salzstress und kann daher unterschiedliche Ökosysteme im Menschen besiedeln wie Blase, Hautoberfläche und Lunge. Die molekulare Basis dieser Anpassungsstrategien wird im Rahmen der Forschungsgruppe (FOR) 2251 der Deutschen Forschungsgemeinschaft, dessen Sprecher Prof. Volker Müller von der Goethe Universität ist, seit 2017 untersucht.
Nun hat das Wissenschaftsteam um die beiden FOR2251-Teilprojektleiter Prof. Beate Averhoff und Prof. Volker Müller einen zuvor bei Acinetobacter unbekannten Mechanismus der Anpassung entdeckt. Viele Bakterien gehen bei unwirtlichen Lebensbedingungen in einen fast todesähnlichen Ruhezustand über: Sie entwickeln Dauerformen ohne jegliche Stoffwechselaktivität, so genannte Sporen.
Acinetobacter baumannii kann jedoch, so fand das Wissenschaftsteam heraus, alternativ auch spezielle Zellen ausbilden, die sich in einer Art Tiefschlaf befinden. Diese Zellen zeigen zwar noch Lebenszeichen und atmen, lassen sich aber auf Nährböden in Petrischalen nicht mehr kultivieren. „Dieser Zustand ist beispielsweise von Cholerabakterien bekannt und wird viable but non-culturable (VBNC) genannt“, erklärt Müller. In diesem Zustand können die Bakterien lange überdauern, berichtet Patricia König, die Erstautorin der Studie, die jetzt in der renommierten Zeitschrift mBio publiziert wurde: „Wir halten die Bakterien mittlerweile seit elf Monaten im VBNC-Tiefschlaf und überprüfen immer wieder, ob wir sie noch aufwecken können. Die Untersuchung läuft noch und ein Ende ist noch nicht in Sicht.“
Auslösen konnten die Wissenschaftler:innen den VBNC-Zustand der Acinetobacter-Bakterien durch einen hohen Salzgehalt des Kulturmediums, daneben aber auch – zeitverzögert – durch Kühlschrank- (4 Grad Celsius) und Fiebertemperaturen (42 Grad Celsius), durch Austrocknung und durch Sauerstoffmangel. In allen Fällen gelang es, die Bakterien nach einer zweitägigen „Kur“ im Bakterienschüttler unter optimalen Nähr- und Sauerstoffversorgung wieder „aufzuwecken“.
Das Problem: In der Medizin wie auch in der Lebensmittelüberwachung ist der Nachweis von Bakterien durch Kultivierung auf Nährböden immer noch der Goldstandard. Beate Averhoff erläutert: „Man stelle sich Folgendes vor: Ein Patient mit einer Acinetobacter-baumannii-Infektion bekommt eine Antibiotika-Behandlung, und nach sieben Tagen wachsen auf den Kulturschalen keine Acinetobacter-Bakterien mehr. Arzt und Patient gehen davon aus, dass das Bakterium verschwunden ist, aber in Wirklichkeit schläft es nur in Nischen des Körpers und wartet darauf, bei nächster, besserer Gelegenheit wieder aufzuwachen, sich zu vermehren und erneut Symptome im Patienten hervorzurufen. Das ist insbesondere bei multiresistenten Bakterien äußerst gefährlich.“
Patricia König meint: „Wir hoffen damit beitragen zu können, wirksamere Behandlungskonzepte gegen Acinetobacter baumannii entwickeln zu können. Vor allen Dingen müssen neben der Kulturschalen auch sensitivere Verfahren wie zum Beispiel PCR zum Nachweis von Acinetobacter baumannii eingesetzt werden, mit denen man auch VBNC-Zellen entdecken kann.“
Therapeutisch könnten neue Ansatzpunkte in den Proteinen liegen, die beim Übergang in den Dornröschenschlaf eine wichtige Rolle zu spielen scheinen. Eine Reihe solcher Proteine konnte das Wissenschaftsteam bereits identifizieren. König sagt: „Die Rolle dieser Proteine müssen wir verstehen lernen. Auf dieser Basis können sich dann Hemmstoffe dagegen entwickeln lassen, die man zusammen mit Antibiotika verabreichen kann, um den gefährlichen Dornröschenschlaf der Bakterien zu verhindern.“
Publikation: Patricia König, Alexander Wilhelm, Christoph Schaudinn, Anja Poehlein, Rolf Daniel, Marek Widera, Beate Averhoff, Volker Müller. The VBNC state: a fundamental survival strategy for Acinetobacter baumannii. mBio (2023) https://doi.org/10.1128/mbio.02139-23 .













