„Mehr Licht!“ – so lauteten, glaubt man seinem Arzt Carl Vogel, die letzten Worte des größten deutschen Dichters und Denkers Johann Wolfgang Goethe. Aus der Sicht der Fluoreszenzmikroskopie ist das kein guter Grundsatz. Die Kernidee der Lichtscheiben-Fluoreszenzmikroskopie (LSFM) liegt in der Macht der dunklen Seite. Anders gesagt: Sie folgt dem Prinzip, dass weniger manchmal viel mehr sein kann. Die schonende Beleuchtung empfindlicher Proben bei der LSFM birgt großes Potenzial für die moderne Zell- und Entwicklungsbiologie.
Die Fluoreszenzmikroskopie beruht auf dem Prinzip, leuchtfähige Moleküle (Fluorophore) in einer Probe anzuregen und sie anhand des Lichts, das sie spontan aussenden, mit hoher Genauigkeit zu orten. Das Licht für die Anregung hat dabei eine andere Wellenlänge als das Fluoreszenzlicht. In einem konventionellen oder konfokalen Epifluoreszenzmikroskop durchdringt das Anregungslicht die gesamte Probe und regt (aufgrund der Energieerhaltung)in jeder Ebene die gleiche Anzahl von Fluorophoren an. Um einen dreidimensionalen Datensatz aufzuzeichnen, sammelt man das Fluoreszenzlicht verschiedener Schichten ein, indem man mit dem Fokus von der Oberfläche der Probe in die Tiefe wandert. Das bedeutet, dass bei jeder Aufnahme nicht nur die Fluorophore in der fokussierten Ebene angeregt werden, sondern alle Fluorophore in der Probe. Benötigt man zum Beispiel 100 Aufnahmen, um einen dreidimensionalen Datensatz aufzuzeichnen, dann wurden die Fluorophore in der Mitte (also in der fünfzigsten Ebene), bereits 49-mal angeregt, bis sie im Fokus liegen.
[dt_call_to_action content_size=“normal“ background=“fancy“ line=“true“ animation=“fadeIn“]
Fundamentale Grenzen der Fluoreszenzmikroskopie
- Fluorophore bleichen und werden während eines Experimentes verbraucht.
- Viele metabolisch relevante endogene Moleküle absorbieren das gleiche Anregungslicht und werden ebenfalls abgebaut.
- Die Anzahl der Fluorophore ist begrenzt und kann nicht beliebig erhöht werden.
- Aus 1 und 3 folgt, dass die Anzahl der für die Bildgebung verfügbaren Photonen begrenzt ist.
- Eine physiologisch akzeptable Belastung lässt sich über die Solarkonstante (circa 1,4 kW/m²) abschätzen und sollte in einem Mikroskop unter 1 nW/μm² beziehungsweise unter 100 mW/cm² liegen.
[/dt_call_to_action]
Seit einigen Jahren heißt die Alternative: Statt eine Probe am Stück zu beleuchten und zu beobachten, werden Anregungen und Aufnahmen »scheibenweise« durchgeführt. Ein Lichtscheibenfluoreszenzmikroskop (LSFM) besteht in erster Linie aus einer Beobachtungseinheit, die der eines Epifluoreszenzmikroskops sehr stark ähnelt. Das Fluoreszenzlicht wird mit einem Mikroskopobjektiv, einem Fluoreszenzfilter, einer Tubuslinse und schließlich einer Kamera aufgenommen. Es fehlt der dichroitische Spiegel, der das Anregungslicht herausfiltert, da dieses nicht über das gleiche Mikroskopobjektiv eingekoppelt wird und damit auch nicht von oben (gr. epi) in die Probe fällt. Das Besondere an einem LSFM ist, dass das Anregungslicht über einen zweiten, unabhängigen Lichtpfad geführt wird und von der Seite in die Probe einstrahlt. Eine Zylinderlinse formt aus dem Lichtstrahl eine Scheibe beziehungsweise ein Blatt, das sich eng um die Fokalebene der Beobachtungsoptik schmiegt (Abb. 1). Das hat zur Folge, dass nur die Fluorophore angeregt werden, die sich in der Fokalebene befinden. Fluorophore, die, von dem Mikroskopobjektiv der Beobachtungsoptik aus gesehen, vor oder hinter dieser Ebene liegen, empfangen kein Licht und werden nicht angeregt. Sie können deshalb weder ausbleichen noch zum Bild beitragen.
Der größte Vorteil der LSFM ist, dass ausschließlich der Probenanteil beleuchtet wird, der sich in der Fokalebene des Detektionssystems befindet. Der hieraus resultierende »Gewinn« für die Probe lässt sich in Zahlen fassen. Er ergibt sich aus dem Verhältnis von Proben- und Lichtscheibendicke und liegt zwischen etwa zehn für Hefe und mehreren Hundert für Fruchtfliegen- und Zebrafischembryonen. Da konfokale Fluoreszenzmikroskope zudem eine Lochblende benötigen und ihre Detektoren nicht so effizient sind wie moderne Kameras, ist ein zusätzlicher Faktor der Belastung mit Lichtenergie von fünf bis fünfzehn zu berücksichtigen.
Als noch recht junge Methode erweist sich LSFM vor allem in der Langzeitbeobachtung von dreidimensionalen (3D) lebenden Proben als besonders vorteilhaft. So finden sich immer mehr Publikationen in verschiedenen Bereichen der Zell- und Entwicklungsbiologie, in denen die besonderen Vorteile von LSFM genutzt werden.
Sphäroide als Tumormodell
In der 3D-Zellbiologie werden häufig Sphäroide (Aggregate miteinander interagierender Zellen) als Modell verwendet. Sie werden aus mehreren Zellen geformt, die in einer nicht-adhäsiven Umgebung Zell-Zell-Kontakte ausbilden. Im Prinzip können die meisten Zelltypen (zum Beispiel Primärzellen, Tumorzelllinien und »herkömmliche« Zelllinien) Sphäroide bilden. In der Praxis gibt es unterschiedliche Methoden, sie zu erzeugen. Bei der Tropfen-Methode werden vereinzelte Zellen in einem Tropfen Medium auf eine nicht haftende Fläche pipettiert, die dann kopfüber im Zellinkubator platziert wird. Die Zellen kommen, dank der Schwerkraft, am unteren Teil des Tropfens zusammen und bilden ein Aggregat. Eine andere Methode besteht darin, die Zellsuspension in Agarosebeschichtete oder nicht haftende, U-förmige Vertiefungen von Mikrotiterplatten zu pipettieren (Abb. 2a). Darin formen die vereinzelten Zellen im Verlauf von mehreren Stunden bis Tagen kompakte Sphäroide (Abb. 2b).
Der Sphäroid kann also bei Langzeit-Lebendaufnahmen optimal versorgt werden. Kurzum, durch die reduzierte Phototoxizität, das verminderte Bleichen der Fluorophore sowie die hohe Aufnahmegeschwindigkeit bietet LSFM eine gute Möglichkeit, Sphäroide über einen längeren Zeitraum zu untersuchen. Abbildung 3a zeigt Bilder eines aus T47D-Brustkrebszellen geformten Sphäroids.
Sphäroide werden als Tumormodell verwendet und finden in der Wirkstoffsuche immer mehr Anklang, da sie den physiologischen Zustand eher repräsentieren als ein zweidimensionaler »Zellrasen «, der auf einer harten Plastikoberfläche gewachsen ist. Für die Tumorforschung ist eine detaillierte Beobachtung von Sphäroiden unerlässlich. Lichtscheibenmikroskopie ist dabei eine gute Wahl, da Endpunktaufnahmen, die einen Blick ins Innere der Sphäroide gestatten, mit sehr guter Qualität und hoher Eindringtiefe angefertigt werden können. Lebende Sphäroide lassen sich mit LSFM auch über längere Zeiträume hinweg beobachten, da Effekte wie Schädigung durch Licht (Phototoxizität) und Bleichen auf ein Minimum reduziert sind.
[vc_row][vc_column][vc_accordion active_tab=“false“ title_size=“h3″ style=“3″][vc_accordion_tab title=“Abbildung 1″][vc_column_text]
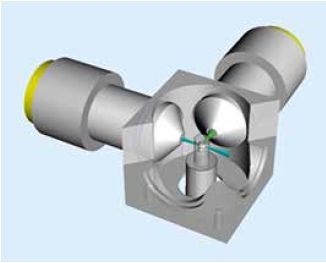
Schematische Darstellung der LSFM. Eine biologische Probe befindet sich innerhalb eines Zylinders. Sie wird seitlich mit einer Lichtscheibe (zyan) bestrahlt. Das Fluoreszenzlicht (grün) wird in einem Winkel von 90° erfasst.[/vc_column_text][/vc_accordion_tab][vc_accordion_tab title=“Abbildung 2″][vc_column_text]
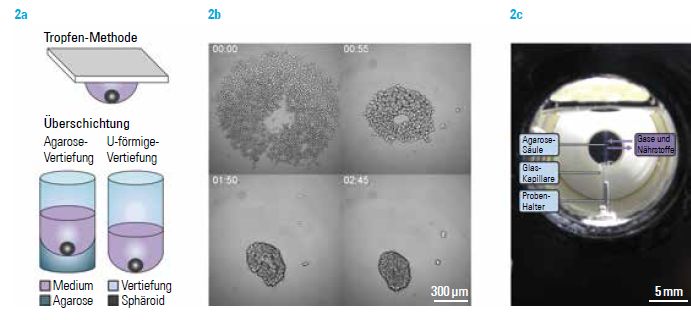
Formierung und Präparation von Sphäroiden
2a Schematische Darstellung der Tropfen-Methode und der Überschichtung, die zur Formierung von Sphäroiden aus einzelnen Zellen eingesetzt werden.
2b Formierung eines Sphäroiden aus 2.000 Einzelzellen über etwa drei Stunden.
2c LSFM-Probenkammer in der Frontalansicht auf das Detektionsobjektiv mit einem Sphäroiden, der in eine Agarosesäule eingebettet ist.[/vc_column_text][/vc_accordion_tab][vc_accordion_tab title=“Abbildung 3″][vc_column_text]
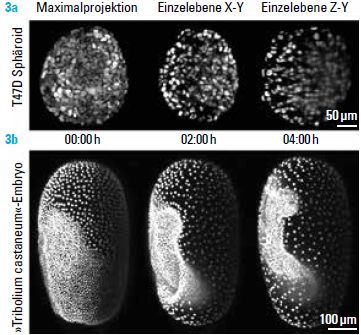
LSFM-Aufnahmen eines Sphäroiden und eines Rotbraunen Reismehlkäfer Embryos (»Tribolium-castaneum«)
3a Der Sphäroid wurde aus 300 Brustkrebszellen geformt, in denen die Zellkerne mit einem fluoreszierenden Farbstoff markiert sind. Er wird als Projektion des Bildstapels und in zwei Einzelebenen entlang unterschiedlicher Achsen dargestellt.
3b Lebendaufnahme der Gastrulation eines transgenen »Tribolium castaneum«-Embryos. Gezeigt werden Projektionen an drei
Zeitpunkten. Man sieht, wie sich die Keimblätter entwickeln. Der Käfer hat die Aufnahmedauer von 50 Stunden ohne sichtbare Schäden überlebt und Nachkommen erzeugt. Insgesamt wurden mehr als 200 Stapel zu jeweils 170 Bildern und entlang jeweils vier Raumrichtungen aufgenommen. Das entspricht mehr als 140.000 Bildern beziehungsweise 400 GByte.[/vc_column_text][/vc_accordion_tab][vc_accordion_tab title=“Abbildung 4″][vc_column_text]

Beispiele für LSFM-Datenverarbeitung
4a Dreidimensionales Rendering eines T47D-Sphäroiden mit Mathematica und eines »Tribolium castaneum«-Embryos mit Amira.
4b Dreidimensionale Segmentierung eines T47D-Sphäroids bestehend aus etwa 5000 Zellen.[/vc_column_text][/vc_accordion_tab][/vc_accordion][/vc_column][/vc_row]
Wie bekomme ich den Sphäroid in ein LSFM? Hier bieten sich je nach Fragestellung verschiedene Arten der Präparation an. Die klassische Methode ist die Präparation der Probe in einer Agarosesäule, die dann in die LSFM-Probenkammer gesetzt wird (Abb. 2c). Hierfür wird der Sphäroid zunächst in lauwarme flüssige Agarose, einen Gelbildner, überführt und dann in eine Glaskapillare aufgezogen. Nachdem die Agarose ausgehärtet ist, wird sie so zurechtgeschnitten, dass sie auf den Probenhalter im Mikroskop gesteckt werden kann. Ein dünner Stift an der Oberseite des Probenhalters wird in die Kapillare geführt und drückt den Teil der Agarosesäule, in dem sich der Sphäroid befindet, am anderen Ende heraus. Die polymerisierte Agarose fungiert als engmaschiges Netz, das für Stabilität sorgt und den Sphäroid während der Aufnahme in seiner Position hält. Zusätzlich erlaubt die Agarose den Austausch von Gasen und Nährstoffen mit dem in der Probenkammer befindlichem Medium.
Wachsende Embryonen in 3-D beobachten
Ein zweites großes Anwendungsfeld von LSFM ist die Entwicklungsbiologie. Während des letzten Jahrzehnts haben sich mehrere Techniken für das Beobachten von Embryonen etabliert und neue Modellorganismen durchgesetzt. Einer der wichtigsten Faktoren bei der Untersuchung von Entwicklungsprozessen ist, die dreidimensionale Integrität der Probe zu bewahren und deren Wachstum nicht zu behindern. Ähnlich wie bei Sphäroiden können Embryonen in Agarosesäulen eingebettet werden, was für einige Organismen (etwa bei der Fruchtliege, Drosophila melanogaster) problemlos funktioniert. Bei Tribolium castaneum, dem Rotbraunen Reismehlkäfer, hat sich eine andere Technik als Erfolg versprechend erwiesen: Der Embryo wird kopfüber auf die Spitze einer Agarose-Halbkugel »geklebt«. Der Einsatz von Teflonröhrchen erlaubt es, Zebrafisch-Embryonen in sehr niedrig konzentrierter Agarose einzubetten und dadurch den Einfluss auf das Größenwachstum zu minimieren. Auch Mäuseembryonen wurden schon mit LSFM beobachtet. Hierfür wurde ein Acrylstab mit kleinen »Taschen« verwendet, in die die Embryonen platziert wurden. Alle genannten Techniken für die Aufnahme im LSFM haben eines gemeinsam: Statt die Probe, wie in der konventionellen Mikroskopie, an das Mikroskop anzupassen, werden bei LSFM die Präparation und das Mikroskop an die Probe angepasst.
Wie bekommt man einen Embryo nun zum »Leuchten«? Letztlich haben sich drei grundlegende Standards etabliert, die bei den meisten Modellorganismen der Entwicklungsbiologie geläufig und mit LSFM kompatibel sind: (1) Die Injektion oder Applikation von fluoreszierenden Farbstoffen, (2) die Injektion oder Applikation von Boten-RNA (mRNA), die für Fluoreszenzproteine kodiert, und (3) die Herstellung von transgenen Organismen, die Fluoreszenzproteine exprimieren. Die ersten beiden Methoden lassen sich verhältnismäßig schnell umsetzen, erfordern aber Manipulationen der Probe. Expressionsort und Zeitfenster lassen sich nur bedingt beeinflussen. Bei der letztgenannten Methode müssen im Vorfeld mehr Zeit und Arbeit investiert werden. Dafür kann die Probe ohne weitere Vorbereitung in das Mikroskop gesetzt werden. Expressionsort und Zeitfenster lassen sich unabhängig festgelegen. Gerade der Aspekt der hohen zeitlichen Auflösung kombiniert mit geringer Phototoxizität und Bleichen machen LSFM zu einer idealen Methode für Langzeit-Lebendbeobachtungen in der Entwicklungsbiologie. Bei der Arbeit mit lebenden, sich über mehrere Stunden, Tage oder sogar Wochen entwickelnden Proben ist es äußerst wichtig, dass der Einfluss der Beobachtungsmethode auf die Probe minimiert wird.
Deshalb ist es auch wichtig, stringente Qualitätsstandards für die Arbeit festzulegen. Bei der Beobachtung von Insektenembryonen wird der Embryo nach der Aufnahme unter physiologischen Bedingungen weiter inkubiert und anschließend überprüft, ob er schlüpft, sich zum gesunden Tier entwickelt und Nachkommen zeugen kann. Nur so wird sichergestellt, dass durch den Energieeintrag während der Aufnahme keine Schäden am untersuchten Objekt hervorgerufen wurden und dass die Aufnahme die Wildtyp-Entwicklung abbildet. Eine Beispielaufnahme von drei Zeitpunkten während der Gastrulation des Rotbraunen Reismehlkäfers Tribolium castaneum ist in Abbildung 3b gezeigt. Die Gastrulation ist eine der wichtigsten Phasen der Embryonalentwicklung, bei der sich die drei Keimblätter bilden. Jedes Keimblatt hat im weiteren Verlauf der Embryogenese eine andere Funktion: Aus dem äußeren entsteht beispielsweise das Nervensystem, aus dem mittleren die glatte Muskulatur und aus dem inneren das Verdauungssystem.
Suche nach der Stecknadel im Datenhaufen
Eine große Herausforderung in der Anwendung der LSFM in der Zell- und Entwicklungsbiologie besteht darin, die multidimensionalen Daten zu visualisieren und zu verarbeiten. Üblicherweise liegt der Umfang einer Aufnahme für ein Experiment schnell im Bereich von mehreren 100 Gigabyte bis zu einigen Terabyte. Für die Beobachtung der Embryogenese von Tribolium castaneum über einen Zeitraum von fünf Tagen wird bereits circa 1 Terabyte an Bildern generiert. Der Experimentator muss daher einiges beachten: (1) Aufgrund der Menge lassen sich die Daten nur begrenzt über längere Zeiträume abspeichern. (2) Komplexität und Umfang der Daten machen aus der Analyse eines untersuchten Prozesses das sprichwörtliche Suchen nach der »Stecknadel im Heuhaufen«. (3) Die Leistung vieler Rechensysteme reicht häufig nicht aus, um eine Verarbeitung in einem vernünftigen zeitlichen Rahmen zu ermöglichen. (4) Es bedarf einer Folge von spezialisierten Programmen für die Extraktion der relevanten Information. Aus diesen Gründen gestaltet sich die qualitative und quantitative Auswertung der Daten als komplex und zeitaufwendig. Schnelle, automatisierte Verarbeitungsabläufe und Programme sind also gerade für LSFM essenziell.
Glücklicherweise schreitet die Entwicklung leistungsfähiger Systeme für die Datenverarbeitung stetig voran. Schnelle, mehrkernige Prozessoren, große Arbeits- und Festplattenspeicher, schnelle Flashspeicher und die Möglichkeit, auf massiv parallel arbeitenden Grafikkarten zu rechnen, gehören heute zum Standard vieler Arbeitsgruppen und ermöglichen es, viele Terabyte große Datensätze zu verarbeiten. Computer-Cluster sind zudem häufig arbeitsgruppenübergreifend vorhanden und deutlich leichter zu nutzen als noch vor einigen Jahren. Für die Visualisierung existiert eine Gruppe von kommerziellen, hoch spezialisierten Programmen, die es erlauben, Terabyte große 3-D-Datensätze als Funktion der Zeit darzustellen. Damit ist es möglich, einen fundierten Einblick in die Daten zu bekommen, aber auch, sie Nichtexperten leichter zugänglich zu machen. Abbildung 4a zeigt beispielhaft gerenderte Bilder eines Sphäroids und eines Tribolium castaneum-Embryos.
Mittlerweile existiert eine Vielzahl frei zugänglicher Programme für die Bildverarbeitung. Hierzu zählen die frei verfügbaren Programme Fiji, Icy, Cell Profiler oder Ilastik. Siebieten Basisfunktionen, aber auch spezialisierte Erweiterungen für einige der gängigsten Verarbeitungsschritte an. Sofern die Bildverarbeitung in eine Analysefolge eingebettet werden soll, bedarf es jedoch meist umfangreicherer Programme. Hier bieten kommerzielle Plattformen wie Mathematica oder Matlab neben zahlreichen Möglichkeiten für die Bildverarbeitung auch Funktionen für die weiterführende statistische Auswertung und Analyse. Die Qualität der Aufnahmen mit LSFM ermöglicht eine umfangreiche quantitative Datenanalyse: Die automatische Erkennung von Objekten in Bildern (Segmentierung) kann auf zellulärer und subzellulärer Ebene durchgeführt werden. Anschließend können Merkmale von Zellen und Organellen extrahiert werden. Dank der hohen zeitlichen Auflösung können Zellen und Strukturen über längere Zeiträume verfolgt und zelluläre Stammbäume rekonstruiert werden. Abbildung 4b zeigt beispielhaft die Segmentierung aller Zellkerne eines Sphäroids.
Allerdings erfordern die vielen unterschiedlichen Anwendungen eine stetige Neu- und Weiterentwicklung von Algorithmen und Programmen für die Bildverarbeitung. Aus den Bedürfnissen der Verarbeitung der aufgenommenen Bilddaten entstehen völlig neue Arbeitsfelder, in denen sich Fachleute aus den Bereichen Informatik, Bioinformatik, Mathematik und Physik auf die Verarbeitung und Auswertung biologischer Bilddaten spezialisieren.
Die angeführten Aspekte zeigen das hohe Potenzial und die Wichtigkeit von LSFM im Bereich der Zell- und Entwicklungsbiologie. Allerdings ist LSFM noch ein sehr junges Feld, und wir haben grade erst begonnen, ihr Potenzial auszuschöpfen. Wir dürfen uns also sicherlich in den nächsten Jahren auf sehr spannende Entwicklungen freuen.
[dt_call_to_action content_size=“small“ background=“fancy“ line=“true“ animation=“fadeIn“]
Die Autoren
Prof. Dr. Ernst H. K. Stelzer (2. von links), geboren 1959, studierte Physik und arbeitete von 1979 bis 1983 am Max-Planck-Institut für Biophysik. Seine Doktorarbeit schloss er 1987 am EMBL in Heidelberg ab. Insgesamt arbeitete er 28 Jahre als Wissenschaftler am EMBL in den Bereichen Physikalische Optik, Biophysik, Zellbiologie und Entwicklungsbiologie. Er entwickelte neue Ansätze zur modernen Mikroskopie, die in biologischen Projekten zur Anwendung kommen. Seit 2011 nimmt er einen Ruf auf eine W3-Professur in der Physikalischen Biologie wahr. Sein Labor ist am Buchmann Institut angesiedelt. ernst.stelzer@physikalischebiologie.de

Katharina Hötte (links) und Isabell Smyrek sind Zellbiologie-Doktorandinnen und arbeiten daran, die Methodik der dreidimensionalen Zellkultur zur verfeinern und alternative Modelsysteme zu Tierversuchen zu etablieren. Frederic Strobl (Mitte) ist Doktorand für Entwicklungsbiologie und vergleicht die Embryonalentwicklung mehrerer Insektenspezies, indem er genetische Werkzeuge mit moderner Mikroskopie verbindet. Alexander Schmitz ist Bioinformatik-Doktorand und beschäftigt sich mit der quantitativen Auswertung von Mikroskopiedaten, indem er Algorithmen für die Erkennung und Analyse subzellulärer Strukturen entwickelt.
[/dt_call_to_action]
Der Artikel ist erschienen in „Forschung Frankfurt“ 2/2015: „Die Macht der dunklen Seite„.