Copyright: American Society of Microbiolgy
Frankfurter Wissenschaftler haben ein neuartiges Verfahren zur Untersuchung von bakteriellen Infektionen mittels menschlichen Gewebes erstmalig erfolgreich eingesetzt. Die Methode hat das Potenzial, bei verschiedenen medizinischen Forschungsfragen einen Ersatz für Tierversuche zu bieten – mit noch präziseren Ergebnissen.
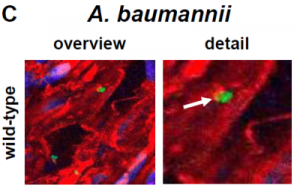
Ein Forschungsteam unter der Leitung von Prof. Volkhard Kempf, Direktor des Instituts für Medizinische Mikrobiologie und Krankenhaushygiene, fand heraus, dass bestimmte bakterielle Infektionen an Nabelschnurgewebe simuliert werden können. Dabei lassen sich realistischere Ergebnisse als bei den bisher genutzten Zellkur- oder Tierversuchen erzielen. Nabelschnurgewebe eignet sich besonders gut für diese Simulation, da mit seiner Hilfe der menschliche Blutfluss imitiert wird und so Infektionsbedingungen ex vivo (also außerhalb des menschlichen Körpers) nachgestellt werden können. Die Forscher untersuchten, wie sich Bartonella henselae, ein von Katzen auf den Menschen übertragenes Bakterium, sowie der gefährliche Krankenhauskeim Acinetobacter baumannii an Blutgefäßzellen anheften. Dies stellt eine der zentralen Phasen der Infektion dar. Im nächsten Schritt werden die Frankfurter Forscher das Modell dazu nutzen, die Reaktion der Blutgefäße auf eine bakterielle Infektion zu analysieren. „Dieses neue Testverfahren könnte die experimentelle Grundlage für neue antiinfektive Therapien legen und die medizinische Forschungspraxis wesentlich beeinflussen“, sagt Prof. Kempf.
Realistisch und ethisch unbedenklich
Copyright: American Society of Microbiolgy
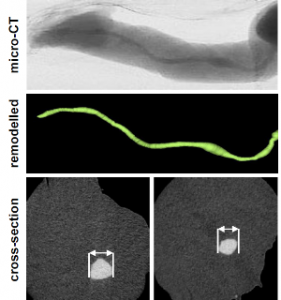
Normalerweise wird das Gewebe der Nabelschnur nach der Geburt entsorgt. Mit der neuen Methode wurden die in den Nabelschnüren vorhandenen Blutgefäße stattdessen dazu genutzt, die krankmachenden Eigenschaften von Bartonella henselae und Acinetobacter baumannii zu analysieren. Dafür schnitten die Wissenschaftler die Nabelschnur in zwei Stücke von ca. fünf Zentimetern Länge. Die Venen des Gewebes verbanden sie mit einer Art Schlauchsystem, um einen Blutfluss zu erzeugen. Durch diese Venen leiteten sie dann Bakterien sowie genetisch modifizierte Erreger und untersuchten das Ausmaß der Anheftung an die Innenseite der Blutgefäße. Das Verfahren hat mehrere Vorzüge: Menschliche Nabelschüre sind in großer Zahl verfügbar und lassen sich problemlos für die Forschung nutzen. In ihren Venen kann ein konstanter Blutfluss erzeugt werden, der den Bedingungen im menschlichen Körper entspricht. Prof. Kempf sieht daher großes Potenzial: „Wir konnten in unseren Untersuchungen belegen, dass dieses Infektionsmodell sehr gut die Infektionsbedingungen von Blutgefäßzellen imitiert. Die Bedingungen sind realistischer als Zellkultur- und Tierversuche. Es stellt damit eine vielversprechende und ethisch sehr gut vertretbare Forschungsmethode dar.“
Pressemitteilung der Universitätsklinik
[dt_call_to_action content_size=“small“ background=“fancy“ line=“true“ animation=“fadeIn“]
Publikation
Weidensdorfer, M., Chae, J.I., Makobe, C., Stahl, J., Averhoff, B., Müller, V., Brandes, R.P., Wilharm, G., Ballhorn, W., Christ, S., Linke, D., Goettig, S., Kempf, V.A.J. Analysis of endothelial adherence of Bartonella henselae and Acinetobacter baumannii using a dynamic human ex vivo infection model. Infect Immun. 2015 Dec 28, doi: 10.1128/IAI.01502-15. Abstract
Mehr zu Bartonella henselae, dem Erreger der Katzenkratzkrankheit:
Christiane Beerlage, Fiona O’Rourke und Volkhard A. J. Kempf: Wenn Bartonellen ihre Anker auswerfen: Bartonella henselae verbindet Infektionsforschung mit Blutgefäßwachstum, in: Forschung Frankfurt 2/2011
Pressemitteilung vom 21.7.2011: Wenn Bartonellen ihre Anker auswerfen
[/dt_call_to_action]