Zwei ERC-Advanced Investigator Grant des Europäischen Forschungsrats mit je 2,5 Millionen Euro gehen an Forscher der Goethe-Universität Frankfurt. Der Soziologe Prof. Thomas Lemke erforscht die gesellschaftlichen Auswirkungen der Kryobiologie, die sich mit dem Einfrieren und der dauerhaften Konservierung organischen Materials beschäftigt. Der Biochemiker Prof. Robert Tampé will die verschlungenen Pfade des Immunsystems innerhalb der Zelle aufklären.
Zwei ERC-Advanced Investigator Grant des Europäischen Forschungsrats mit je 2,5 Millionen Euro gehen an Forscher der Goethe-Universität Frankfurt. Der Soziologe Prof. Thomas Lemke erforscht die gesellschaftlichen Auswirkungen der Kryobiologie, die sich mit dem Einfrieren und der dauerhaften Konservierung organischen Materials beschäftigt. Der Biochemiker Prof. Robert Tampé will die verschlungenen Pfade des Immunsystems innerhalb der Zelle aufklären.
Projekt „Cryosocieties“ erforscht „suspendiertes Leben“
Die Kryobiologie hat in den vergangenen Jahrzehnten einen enormen Aufschwung erfahren. Immer mehr Arten von Gewebe und zelluläres Material können eingefroren, gelagert und wieder aufgetaut werden, ohne einen nachweisbaren Verlust an Vitalität. Heute stellen kryobiologische Praktiken nicht nur eine wichtige infrastrukturelle Bedingung für viele medizinische Anwendungen und einen wesentlichen Motor biowissenschaftlicher Innovationen dar, sondern sie bilden zentrale Optionen für individuelle Reproduktionsentscheidungen ebenso wie die Erhaltung der globalen Biodiversität.
„Im Projekt Cryosocieties möchte ich die Auswirkungen der Kryokonservierung auf unser Verständnis des Lebens untersuchen. Ich gehe von der These aus, dass kryobiologische Praktiken eine spezifische Form des Lebens hervorbringen, die ich „suspendiertes Leben“ oder im Englischen „suspended life“ nenne. Sie hält vitale Prozesse in einem Schwebezustand zwischen Leben und Tod, in welchem die biologischen Substanzen weder völlig lebendig noch gänzlich tot sind“, erklärt Prof. Thomas Lemke vom Institut für Soziologie. Ziel des Projekts an der Schnittstelle zwischen Biologie, Soziologie und Technik ist es zu untersuchen, wie Kryopraktiken zeitliche und räumliche Beziehungen und Konfigurationen sowie unser Verständnis von Leben und Tod, Gesundheit und Krankheit, (Un-)Fruchtbarkeit und Nachhaltigkeit verändern.
Lemke und sein Team werden in drei verschiedenen Kontexten untersuchen, wie „suspendiertes Leben“ in aktuellen Praktiken der Kryokonservierung hervorgebracht wird. Die Teilprojekte befassen sich mit dem Einfrieren von Nabelschnurblut als Vorbereitung auf spätere regenerative Therapien, mit der Kryokonservierung von Eizellen für Reproduktionszwecke sowie mit dem Aufbau von Kryobanken für den Erhalt bedrohter oder bereits ausgestorbener Tierarten.
Immunabwehr in der Zelle
Obwohl das Immunsystem eines der komplexesten Systeme des menschlichen Körpers ist, das sich aus vielen verschiedene Zelltypen, Transport- und Botenmoleküle zusammensetzt, gelingt es Krankheitserregern und Krebszellen immer wieder, es auszutricksen. So haben Herpes- und Pocken-Viren ausgefeilte Strategien entwickelt, bestimmte Pfade der Immunabwehr gezielt anzugreifen. Normalerweise werden Viren, die in die Zelle eingedrungen sind, in einer Art Molekül-Schredder (Proteasom) zerlegt und zur Zelloberfläche transportiert, wo sie den T-Zellen des Immunsystems präsentiert werden. Herpes- und Pocken-Viren schaffen es aber, sich in der Zelle zu verstecken, weil sie das Transportmolekül angreifen, das sie an die Oberfläche befördert.
Bisher weiß man, dass Eiweiß-Schnipsel (Peptide) aus dem Proteasom vom einem großen Molekülkomplex und vielen Hilfsmolekülen für ihre Reise an die Zelloberfläche prozessiert werden. Dieser sogenannte Peptid-Lade-Komplex sitzt im „Maschinenraum der Zelle“, dem endoplasmatischen Retikulum. In dem stark gefalteten System von Membran umschlossenen Hohlräumen werden Proteine hergestellt, gefaltet, kontrolliert und für ihre Reise an die Zelloberfläche vorbereitet.
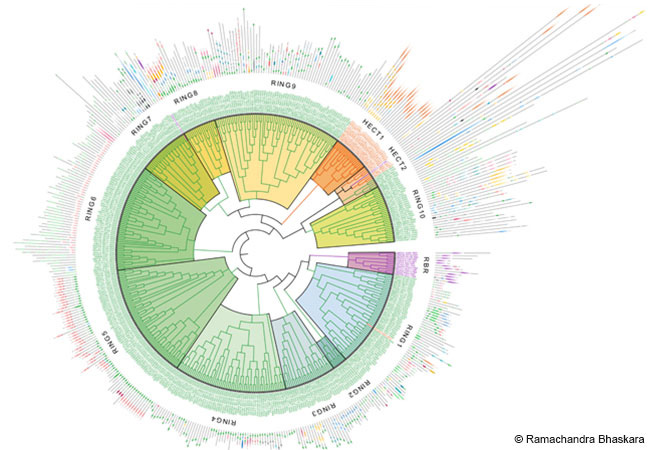
„Mein Ziel ist es, den Mechanismus der Antigen-Prozessierung im Detail zu untersuchen. Mit dieser Forschung begeben wir uns auf einen der dornenreichsten Pfade der Lebenswissenschaften, weil wir es mit großen, unterschiedlich gebauten Molekülen zu tun haben, die außerdem noch relativ selten in interzellulären Membranen vorkommen“, erklärt Prof. Robert Tampé vom Institut für Biochemie das Forschungsvorhaben. Da es seiner Gruppe in den vergangenen Jahren jedoch gelungen ist, einige wichtige Strukturen des Peptid-Lade-Komplexes und deren Funktion aufzuklären, ist er für das neue Forschungsprojekt gut vorbereitet. „Wir erwarten, dass unsere Arbeit einen erheblichen Einfluss auf viele Gebiete der Lebenswissenschaften, insbesondere in Bereich der Krebsforschung sowie Infektions- und Autoimmunkrankheiten haben wird“, so Tampé.