Der Transforming Growth Factor beta (TGF-ß) ist ein Signalprotein, dessen Fehlregulation Entwicklungsstörungen und Krebs hervorrufen kann. Forschende um Dr. Xinlai Cheng von der Goethe-Universität Frankfurt haben herausgefunden, wie ein Tumorsuppressor mit der Kurzbezeichnung pVHL die Signalübertragung mittels TGF-ß beeinflusst. Ihre Erkenntnisse liefern mögliche Ansatzpunkte für neue Medikamente.
Die Signalübertragung in Zellen ist eine komplexe Angelegenheit. So reguliert TGF-ß viele Zellfunktionen während der Entwicklung von Mensch und Tier, aber auch im erwachsenen Organismus. Wie das im Detail funktioniert, ist nur unvollständig bekannt. Klar ist, dass sich aktiviertes TGF-ß zunächst an Rezeptoren bindet, die sich an der Zelloberfläche befinden. Die TGF-ß-Rezeptoren wiederum aktivieren in der Zelle ein Protein namens SMAD3. Dieses lagert sich dann mit SMAD4 zusammen und wandert gemeinsam mit ihm in den Zellkern. Dort beeinflussen die SMAD-Proteine, in welchem Ausmaß Gene angeschaltet und in Proteine und andere Genprodukte übersetzt werden.
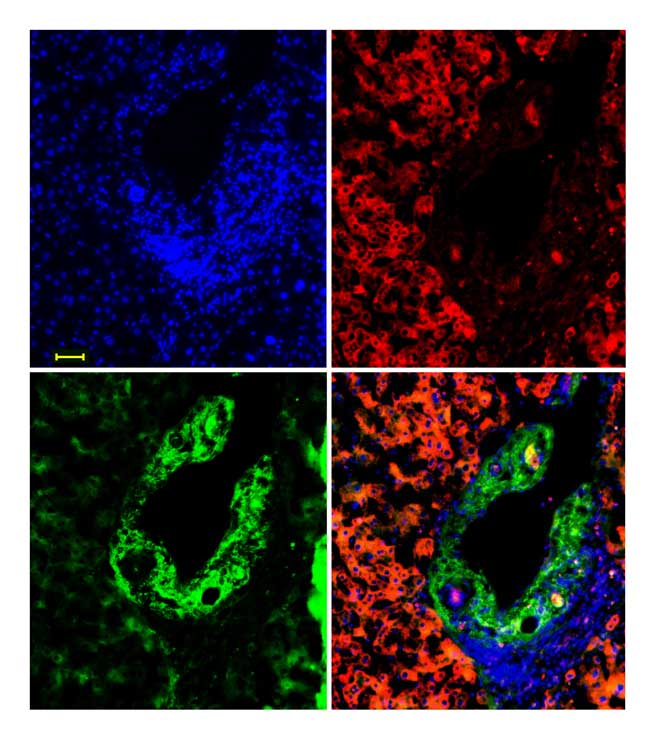
Forschende der Goethe-Universität Frankfurt, der Universität Heidelberg, des Deutschen Krebsforschungszentrums sowie der Universitätskliniken Heidelberg und Jena haben nun herausgefunden, wie der Von-Hippel-Tumorsuppressor (pVHL) in diesen Signalweg eingreift. Tumorsuppressoren sind Proteine, deren Defekt oder Mangel in einem vielzelligen Organismus mit einem hohen Risiko einhergeht, dass Zellen zu Tumorzellen entarten. Die Wissenschaftler berichten im „Journal of Cell Biology“ über den erstmaligen Nachweis, dass pVHL das SMAD3-Protein abbaut. Dies geschieht bereits, bevor sich SMAD3 und SMAD4 verbinden. pVHL hemmt somit die Signalkette, die von aktiviertem TGF-ß ausgeht. „Diesen Nachweis konnten wir sowohl in Kulturen menschlicher Zellen als auch an Taufliegen der Gattung Drosophila erbringen“, sagt Letztautor Dr. Xinlai Cheng. „Das spricht dafür, dass pVHL schon sehr früh in der Evolution die regulierende Funktion übernommen hat, die wir nun aufgedeckt haben.“
Xinlai Cheng ist seit 2019 Leiter einer Nachwuchsgruppe am Buchmann Institut für Molekulare Lebenswissenschaften der Goethe-Universität. Begonnen hatte er die Untersuchungen am Institut für Pharmazie und Molekulare Biotechnologie der Universität Heidelberg. Sein Mentor Prof. Stefan Wölfl erläuterte eine wichtige Erkenntnis, die sich aus dem gefundenen Zusammenhang zwischen pVHL und dem TGF-ß-Signalweg ergibt: „pVHL ist bekanntermaßen daran beteiligt, wie Zellen Sauerstoff gleichsam fühlen und auf dessen unterschiedliche Verfügbarkeit reagieren. Somit beeinflusst die Versorgung von Zellen mit Sauerstoff auch die TGF-ß Signalübertragung.“
Die Entdeckung der Forschenden bietet neue Chancen für die Entwicklung von Medikamenten gegen Krebs. „Könnte man beispielsweise mit einem Wirkstoff die pVHL-Aktivität gezielt regulieren, so würde man darüber auch den TGF-ß Signalweg beeinflussen, der wiederum eine große Rolle bei der Bildung von Tumoren und speziell von Metastasen spielt“, sagt Xinlai Cheng. Tumorzellen können sich gut an ihre Umgebung im Organismus und an unterschiedliche Sauerstoffverfügbarkeiten anpassen. Dabei hilft ihnen, dass sie in ihrer zellulären Aktivität sehr flexibel sind. Diese Aktivität wird unter anderem durch den TGF-ß-Signalweg reguliert.
Publikation: Jun Zhou, Yasamin Dabiri, Rodrigo A. Gama-Brambila, Ghafoory Shahrouz, Mukaddes Altinbay, Arianeb Mehrabi, Mohammad Golriz, Biljana Blagojevic, Stefanie Reuter, Kang Han, Anna Seidel, Ivan Dikic, Stefan Wölfl, Xinlai Cheng: pVHL-mediated SMAD3 degradation suppresses TGFß signalling. Journal of Cell Biology (2022) 221 (1): e202012097 https://doi.org/10.1083/jcb.202012097