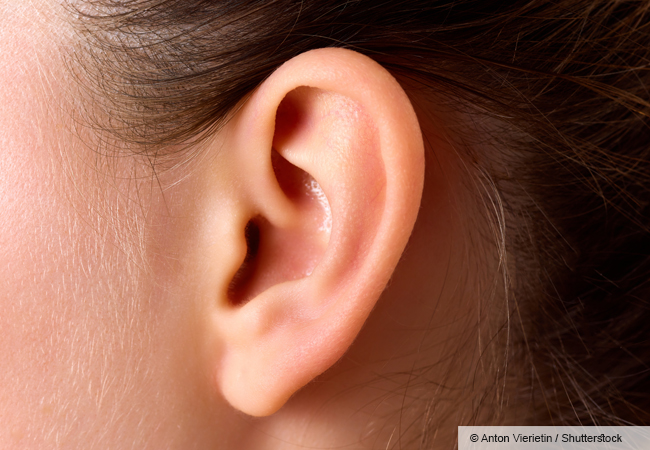
Der Neurophysiologe Jochen Roeper erforscht Morbus Parkinson und Schizophrenie. Dafür sind Tierversuche mit Mäusen notwendig – die Reportage im UniReport schildert, auf welche Weise Verhaltensexperimente mit den Nagern durchgeführt werden.
Zu Besuch bei den Labor-Mäusen: Von den Nagern ist erst einmal nichts zu sehen, befinden sich diese doch in einer Art von High-Tech-Schrank, in dem die Tag- und Nachtzeit simuliert wird. „Wir können den Wach- und Schlafrhythmus der Mäuse umdrehen, sodass unsere Wissenschaftler die nachtaktiven Tiere tagsüber beobachten und versorgen können“, erklärt Prof. Jochen Roeper, geschäftsführender Direktor des Instituts für Neurophysiologie (Physiologie II). Er öffnet einen Schrank und holt eine kleine Kiste hervor, das Zuhause eines Nagers. Die schwarze Maus schaut den Wissenschaftler neugierig an. Wenig Scheu hat das fingergroße Wesen, das gerade einmal 25 Gramm auf die Waage bringt, als Roeper es in die Hand nimmt. „Die hat sich schon an ihr neues Heim gewöhnt“, erklärt er.
Die Maus muss sich wohlfühlen
Wenn die Mäuse vom Züchter angeliefert werden, sind sie in der Regel 6-8 Wochen alt, damit aber bereits erwachsene Tiere. Sie müssen sich dann zuerst einmal an das neue Habitat gewöhnen. Soweit möglich, belässt man die Tiere, meistens Männchen, in Gruppen oder hält sie pärchenweise, denn die Nager sind gesellig. „Mäuse sind zwar neugierige Wesen, benötigen aber immer auch eine gewisse Sicherheit“, betont Roeper. Erst wenn die Maus eine neue Umgebung vertraut geworden ist, kann man auf sinnvolle Weise Verhaltensexperimente mit ihr durchführen. „Wir wollen kognitives und motorisches Verhalten bei den Tieren untersuchen, dafür muss das Tier sich angstfrei verhalten.“ Dazu gehöre auch, dass sie keine Angst vor den Wissenschaftlern und Tierpflegern habe. „Wie man ein Tier richtig anfasst, muss jeder, der in der Forschung arbeitet, zuerst lernen“, betont Dr. Margit Wagenblast, Tierärztin und Tierschutzbeauftragte der Medizin. Dafür sind spezielle Kurse angeboten. Nicht nur Schmerzen können Tiere dazu bringen, zuzubeißen – auch ein falsches Handling kann der Grund dafür sein, weiß die Tierärztin zu berichten. „Es ist jedenfalls ein Mythos, dass Humanmediziner nur aufgrund ihrer Ausbildung schon wüssten, wie man adäquat mit Tieren umgeht“, ergänzt Jochen Roeper.[dt_gap height=“10″ /]
[vc_accordion active_tab=““ collapsible=“yes“ style=“3″][vc_accordion_tab title=“3-R: Neue Tierschutz-Professur an der Goethe-Universität„][vc_column_text]Auch wenn die moderne medizinische Forschung nie vollständig auf tierische Modelle wird verzichten können, ist es möglich, umfangreiche Vorstudien an Tieren mit so genannten In-vitro-Modellen oder auch In-silico Modellen zu ersetzen oder zumindest das Leiden von Tieren quantitativ und qualitativ zu verringern. Diese Strategie wird als „3-R-Strategie“ bezeichnet: Reduction – Refinement – Replacement.
Die Einrichtung einer Stiftungsprofessur an der Goethe-Universität hat das Ziel, neue methodische und technische Konzepte zu entwickeln, die es erlauben, natürliche Zellverbände durch dreidimensionale Zellkulturen realitätsnah nachzuahmen, sodass Tierversuche überflüssig werden (Replacement). Wenn dies nicht ohne weiteres zu erreichen ist, dann bieten standardisierte Protokolle zur Vorbereitung der Versuche (Reduction) bzw. die Optimierung der Experimente (Refinement) Ansatzpunkte der Verminderung der Zahl der Tierexperimente.
„Die Goethe-Universität ist ein herausgehobener Standort der biologischen und medizinischen Grundlagenforschung, der translatorischen Forschung und der klinischen Praxis. Wir sind zudem hervorragend mit außeruniversitären Instituten vernetzt und können auf eine sehr gute Zusammenarbeit mit pharmazeutischen Unternehmen verweisen. Damit ist die Stiftungsprofessur für 3-R-Verfahren, angesiedelt in dem Buchmann Institut für Molekulare Lebenswissenschaften, eingebettet in ein großartig ausgestattetes lokales und ein optimales inspirierendes globales Umfeld“, betont Univizepräsident Prof. Enrico Schleiff. Die Professur wird für fünf Jahre vom Land Hessen gefördert.[/vc_column_text][/vc_accordion_tab][/vc_accordion]
[dt_gap height=“15″ /]Im Institut für Neurophysiologie der Goethe-Universität werden chronische neurologische und psychiatrische Erkrankungen erforscht, zum Beispiel Schizophrenie und Morbus Parkinson. Bei der letztgenannten Erkrankung kommt es altersabhängig zu einem Verlust von Nervenzellen im Gehirn, die Dopamin produzieren. „Eine ausschließliche Erforschung von Parkinson ‚in vitro‘, also im Reagenzglas außerhalb eines lebenden Organismus, ist nicht möglich“, stellt Roeper fest. Mäuse entwickeln zwar spontan keine Parkinson’sche Erkrankung; jedoch ist die Neuroanatomie und Genetik einer Maus dem Menschen so ähnlich, dass sich durch Transfer von beim Menschen identifizierten „Parkinson-Genen“ ein sehr ähnliches Krankheitsbild mit selektivem Absterben der Dopaminneuronen im Mittelhirn erzeugen lässt. Diese eröffnet die Chance, am Mausmodell bereits die allerersten Krankheitsstadien zu identifizieren, was die Früherkennung beim Menschen erleichtert könnte. Neurodegenerative Erkrankungen sind ein Wettlauf mit der Zeit – je früher sie erkannt werden, desto eher kann man therapeutisch – auch neuroprotektiv – eingreifen.
Schmerzvermeidung
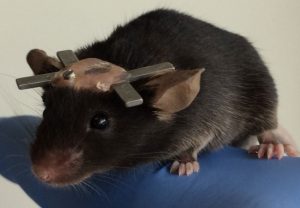
In einem Labor-Raum ist eine junge Wissenschaftlerin aus Roepers Team gerade bei einer Operation: Hochkonzentriert wird der Maus, die narkotisiert auf dem Rücken liegt, ein
kleiner Halter am Schädel befestigt. Damit die Wissenschaftler elektrische Signale aus dem Gehirn der Maus leichter abfragen können, bekommt sie eine Art Interface verpflanzt – „sieht ein bisschen aus wie eine Bischofsmütze“, beschreibt Roeper das für die Maus zuerst einmal fremde Element, an das sie sich aber schnell gewöhnt. Streng sind auch hier die behördlichen Auflagen: Vor der Operation müssen dem Tier ausreichend systemische und lokale Schmerzmittel verabreicht werden.

Zwar ist das Gehirn selbst nicht schmerzempfindlich, aber bei der Operation müssen Schädeldecke und Hirnhaut geöffnet werden. Innerhalb eines Tages, so Roeper, gewöhnt sich die Maus an das neue Element am Kopf und bewegt sich fast ohne Einschränkungen. „Natürlich kann es immer auch mal nach einer Operation zu Komplikationen kommen. Wenn sich das Tier nicht wie erwartet schnell erholt, wird es eingeschläfert.“
Wie Patienten in der benachbarten Klinik, werden die Tiere post-operativ engmaschig überwacht und an Wochenenden und an Feiertagen werden sie täglich „gemonitored“; so muss neben dem Verhalten auch das Körpergewicht genau kontrolliert werden, denn ein zu starker Gewichtsverlust ist bei Mäusen, die einen sehr hohen Stoffwechsel haben, oft ein Indikator für eine Erkrankung. „Es ist eine wirkliche Expertise gefragt, wenn man nach den Tieren schaut. Denn jede Tierart hat ihre Eigenheiten“, unterstreicht Margit Wagenblast. An der Goethe-Universität kommen zwar überwiegend Mäuse und Ratten zum Einsatz, in weitaus geringerem Maße aber auch Fledermäuse, Vögel und Fische sowie Schafe.
»Normalität und Wahnsinn« bei Mäusen
Um Mäuse zur freiwilligen Mitarbeit zu bewegen, müssen sie motiviert werden – meist durch die Möglichkeit, attraktives Futter wie süße Milch oder Zuckerdrops zu erwerben. „Es ist für die Mäuse unattraktiv, ohne Belohnungsmöglichkeit einer Versuchsanordnung länger Aufmerksamkeit zu schenken“, sagt Roeper. Und auch hier greifen Bestimmungen des Tierschutzes, wenn es darum geht, den Tieren für eine begrenzte Zeit Wasser oder Nahrung zu entziehen. „Wir führen die Maus aus einer Rundumversorgung (d. h. unbegrenzter Zugang zu Wasser und Futter), die ja eine künstliche Situation ist und in der freien Natur praktisch nicht vorkommt, in eine des temporären Mangels: Damit weckt man ihr natürliches Interesse an der Nahrungssuche:
Sie lernt, dass sie etwas tun muss, um an Wasser und Nahrung zu kommen, beispielsweise nach bestimmten Regeln in einem Labyrinth nicht rechts, sondern links abzubiegen.“ Laut Tierschutz darf die Maus im Rahmen eines solchen Experiments nicht mehr als 15 Prozent ihres Körpergewichtes verlieren. Wird das Verhalten von Mäusen analysiert, die menschliche Krankheitsgene für Parkinson oder Schizophrenie exprimieren, stellt sich sofort die Frage: Wie definiert sich Normalverhalten, wie abweichendes Verhalten bei einem Lebewesen, dessen Gehirn im Vergleich zum Menschen ähnlich, aber einfacher strukturiert ist?
„Dr. Torfi Sigursson, der im Institut eine unabhängige Arbeitsgruppe leitet, hat z. B. ein Verhaltensparadigma für Mäuse entwickelt, das sich an einem Grundproblem der Schizophrenie beim Menschen orientiert: Kann die Maus zwischen Ereignissen (z. B. der Auslösung eines Tones) unterscheiden, die sie selbst handelnd (z. B. durch Druck einer Taste) in der Umwelt bewirkt, und den gleichen Ereignissen, die ohne ihr Zutun spontan entstehen?“ Diese Grenze zwischen Ich und Welt ist genau das, was bei Schizophrenie oft brüchig wird. „Schizophrene sehen überall Kausalverbindungen, wo aber gar keine vorliegen. Früher waren das oft Einbildungen religiöser Herkunft (der Herr schickt mir Zeichen), heute sind es oft Phänomene aus dem Internet“, schildert Roeper. Ein weit verbreiteter Irrtum sei, dass das Hauptproblem der Schizophrenie vor allem an den akuten psychotischen Schüben läge. Es sind vielmehr die chronischen Einschränkungen der Motivation und der kognitiven Leistungen, die den Alltag und die Chancen der Schizophrenen bestimmen würden.[dt_gap height=“10″ /]
[vc_accordion active_tab=““ collapsible=“yes“ style=“3″][vc_accordion_tab title=“Rhine-Main Neuroscience Network (rmn ²)„][vc_column_text]Prof. Jochen Roeper ist auch Sprecher des „Rhine-Main Neuroscience Networks“ (rmn²), eines der größten und erfolgreichsten Kooperationsprojekte der Rhein-Main-Universitäten (RMU).
Ende Juni trafen sich mehr als 300 Wissenschaftler des Netzwerkes in Oberwesel, um sich über Forschungsergebnisse auszutauschen, Vorträge renommierter Kolleginnen und Kollegen aus dem In- und Ausland zu hören und ihre weitere Arbeit zu planen – wozu unter anderem eine Bewerbung in der nächsten Phase der Exzellenzinitiative gehören soll. Bereits zum dritten Mal nach 2012 und 2014 fand ein solches Treffen des „Rhine-Main Neuroscience Networks“ (rmn²) statt. rmn² wurde vor fünf Jahren offiziell gegründet, um Technologien gemeinsam zu nutzen, neue Erkenntnisse schneller in die klinische Praxis umzusetzen und gemeinsam wissenschaftlichen Nachwuchs auszubilden und zu fördern.
Die Themen des Netzwerkes sind vielfältig und reichen von grundlegenden Fragen zur Bildung neuronaler Netzwerke bis zu anwendungsorientierter Forschung zu Epilepsie oder mentalen Störungen. In einigen Wochen soll der Kooperationsvertrag für die kommenden fünf Jahre unterzeichnet werden. Dann wird neben der Goethe-Universität und der Johannes Gutenberg-Universität Mainz (JGU) auch die Technische Universität Darmstadt als dritte der Rhein-Main-Universitäten beteiligt sein. Außerdem werden das Max-Planck-Institut für Hirnforschung, das Ernst Strüngmann Institute, das Frankfurt Institute for Advanced Studies (FIAS) und das Institut für Molekulare Biologie (IMB) weiterhin als wichtige Partner an Bord sein.
„Die ersten fünf Jahren waren sehr erfolgreich“, sagt Roeper und nennt als Beispiele das Einwerben von zwei Sonderforschungsbereichen der Deutschen Forschungsgemeinschaft (DFG) und die damit verbundene Förderung in zweistelliger Millionenhöhe. Dadurch werde rmn² nun als eines der Zentren der Neurowissenschaften in Deutschland wahrgenommen, könne weiter wachsen und sei hervorragend für Bewerbungen um weitere Fördermittel aufgestellt. Ab dem kommenden Jahr will das Netzwerk an der Exzellenzinitiative teilnehmen. „Die bisherigen Erfolge haben uns zusammengeschweißt und beflügelt. Jetzt freuen wir uns darauf, uns auch diesem Wettbewerb zu stellen“, sagt Roeper. Weitere Informationen: www.rmn2.de[/vc_column_text][/vc_accordion_tab][/vc_accordion]
[dt_gap height=“15″ /]Gerade diesen nur sehr unbefriedigend zu behandelnden Problemen widmen sich die Mausmodelle im Labor. „Daher müssen wir erforschen, wie auch diese Aspekte der Krankheit funktionieren.“ Tiere kommen in der Physiologie nicht nur bei Verhaltensexperimenten zum Einsatz. Um reduktionistische Untersuchungen an Einzelzellen vorzunehmen, werden Tieren auch Organe entnommen. „Das sind per definitionem keine Tierversuche“, unterstreicht Roeper, denn die Tiere werden vorher nach Vorschrift eingeschläfert, erleiden also keine Schmerzen oder sonstige Beeinträchtigungen. Mit den so gewonnenen lebenden Nervenzellen kann man dann einen ganzen Tag arbeiten, bei jungen Tieren sogar länger. Im Mittelpunkt der Arbeitsgruppe steht hier die Hirnschnitt-Technik: Dabei wird dem Gehirn ein bestimmtes Areal entnommen – wie eine dünne „Toastscheibe“, sagt Roeper. So kann man Nervenzellen in vitro, aber dennoch in ihrer lokalen Umgebung untersuchen.
Kontrolle
Soll bei einem wissenschaftlichen Experiment ein Versuchstier zum Einsatz kommen, wird ein Antrag notwendig, der das Vorhaben detailliert beschreibt und begründet. Der Verwaltungsaufwand ist mit zunehmender Sensibilisierung der Gesellschaft für Tierschutz größer geworden. Verschaffen sich die behördlichen Vertreter selber einen Eindruck vor Ort, handelt es sich dabei nicht nur um stichpunktartige Kontrollen? „Der neue europäische Rechtsrahmen sieht viel stärker als früher eine regelmäßige Begehung vor.  Ich bin wissenschaftlich in Großbritannien sozialisiert worden, dort hatte man vor 20 Jahren schon viel schärfere Auflagen als in Deutschland“, sagt Roeper. „Gemäß dem Unerlässlichkeitsprinzip wird von den Behörden nicht nur die fachliche Dimension wie bei einem Forschungsantrag geprüft; hier steht das Tier ganz klar im Fokus, und die Vermeidung von Leid“, erklärt Margit Wagenblast. Sind aber die Behörden denn kompetent genug, die Plausibilität eines Antrages zu begutachten? „Ein Kriterium ist natürlich die bisherige Forschung des Antragstellenden, aber natürlich auch das Vertrauen der Scientific Community beim Gewähren von neuen Drittmitteln“, sagt Roeper. Absolute Gewissheit, ob eine Versuchsreihe zum gewünschten Ziel führe, könne es nicht geben. Grundlagenforschung beinhalte immer eine gewisse Unwägbarkeit. „Das ist manchmal schon fast paradox: Im Vorhinein etwas zu beschreiben, obwohl man gar nicht weiß, in welche Richtung es geht.“ Pilotprojekte in enger Abstimmung mit Behörde seien ein guter Weg, um neue Wege zu erproben.
Ich bin wissenschaftlich in Großbritannien sozialisiert worden, dort hatte man vor 20 Jahren schon viel schärfere Auflagen als in Deutschland“, sagt Roeper. „Gemäß dem Unerlässlichkeitsprinzip wird von den Behörden nicht nur die fachliche Dimension wie bei einem Forschungsantrag geprüft; hier steht das Tier ganz klar im Fokus, und die Vermeidung von Leid“, erklärt Margit Wagenblast. Sind aber die Behörden denn kompetent genug, die Plausibilität eines Antrages zu begutachten? „Ein Kriterium ist natürlich die bisherige Forschung des Antragstellenden, aber natürlich auch das Vertrauen der Scientific Community beim Gewähren von neuen Drittmitteln“, sagt Roeper. Absolute Gewissheit, ob eine Versuchsreihe zum gewünschten Ziel führe, könne es nicht geben. Grundlagenforschung beinhalte immer eine gewisse Unwägbarkeit. „Das ist manchmal schon fast paradox: Im Vorhinein etwas zu beschreiben, obwohl man gar nicht weiß, in welche Richtung es geht.“ Pilotprojekte in enger Abstimmung mit Behörde seien ein guter Weg, um neue Wege zu erproben.
Diskussion in der Gesellschaft
Die zwar nicht mehr ansteigenden, aber auf relativ hohem Niveau verbleibenden Zahlen der zu Forschungszwecken verwendeten Tiere möchte Roeper gar nicht unter den Teppich kehren, sieht aber die Notwendigkeit, die Daten aufzuschlüsseln: „Auch wenn die Zahlen in der Öffentlichkeit sehr kritisch gesehen werden, muss man feststellen, dass sich die Forschung zunehmend dem Prinzip des Reduction und Replacement, also der Reduzierung und dem Ersatz von Tierversuchen durch alternative Methoden, verpflichtet fühlt.[dt_quote type=“pullquote“ layout=“left“ font_size=“h4″ animation=“none“ size=“2″]»„Es ist das legitime Interesse der Wissenschaft, Krankheiten zu verstehen und dadurch das verursachte Leiden für Betroffene und Angehörige zu vermindern.“«[/dt_quote] Man muss die hohen Zahlen in Relation setzen zu dem gesellschaftlich gewünschten Wachstum wissenschaftlicher Erkenntnis. Und vor diesem Hintergrund hat man es keineswegs mit einem exponentiellen Wachstum zu tun.“ Im Zeichen einer zunehmenden Informationsmaximierung würden durch Zusammenarbeit in Forschungsverbünden die Ergebnisse von Versuchen mit Tieren mehrfach genutzt. „Indem man sich auf einige paradigmatische Modelle einigt, wird auch eine höhere Vergleichbarkeit der Ergebnisse sichergestellt“, freut sich Roeper. Die Grundlagenforschung habe es manchmal schwer, sagt Roeper, die Legitimität ihres Handelns deutlich zu machen. Viele Tierversuchskritiker argumentierten: Es gebe doch schon genug Wissen, das man einfach nur anzuwenden bräuchte. Roeper hält dagegen: „Es ist das legitime Interesse der Wissenschaft, Krankheiten zu verstehen und dadurch das verursachte Leiden für Betroffene und Angehörige zu vermindern.“
[dt_call_to_action content_size=“small“ background=“plain“ line=“true“ style=“1″ animation=“fadeIn“]

Prof. Dieter Birnbacher, Tierversuche – die Sicht eines Ethikers
Die Debatte um die Zulässigkeit und die Grenzen von wissenschaftlichen Tierversuchen ist keine neue Debatte. Sie wird spätestens seit dem 17. Jahrhundert geführt, mit – wie etwa der Briefwechsel zwischen René Descartes mit seinem englischen Briefpartner Henry More zeigt – ähnlichen Positionierungen, wie wir sie heute finden. …mehr
[/dt_call_to_action]
Roeper kann seine pathozentrische, also leidensvermeidende Tierschutzposition am Tod Muhammed Alis festmachen, der weltweit für Trauer gesorgt hat: „20 Jahre litt dieser großartige Bewegungskünstler an Morbus Parkinson – an einer Krankheit, die unheilbar ist, die wir aber irgendwann verstehen werden können.“ Neue Erkenntnisse zu gewinnen in den Lebenswissenschaften könne einer der großen Innovations-Motoren der Gesellschaft sein. Dabei hat Roeper nicht allein die sozioökonomische Dimension im Blick. Wenn Roeper über Treibjagden spricht, die extreme Tierversuchsgegner gegen Kollegen initiiert hätten, merkt man ihm zwar seine persönliche Betroffenheit an. Roeper möchte sich aber durchaus der Diskussion stellen: So moderiert er als derzeitiger Sprecher des Rhine-Main Neuroscience Networks (rmn2) regelmäßig eine öffentliche Vortragsreihe zur Neuroforschung, bei denen auch der Einsatz von Tierversuchen immer wieder kontrovers diskutiert wird. „Neben dem durchaus kritischen Dialog zum Einzelantrag zwischen Forscher und Tierschutzbehörde ist auch eine öffentliche Debatte über Tierversuche wichtig und immer dann fruchtbar, wenn beide Seiten an einer sachlichen Debatte interessiert sind und auch gewillt sind, menschliches Leid durch chronische Erkrankungen nicht einfach auszublenden,“ resümiert Roeper.
Dieser Artikel ist in der Ausgabe 4-2016 des UniReport erschienen [PDF].