Was tun, wenn das Immunsystem nicht mehr zwischen fremden und eigenen Zellen unterscheiden kann? Bei Diabetes Typ 1, einer der häufigsten Autoimmunerkrankungen, gibt es bisher keine Heilung. Besonders schwierig wird die Therapie, wenn parallel dazu weitere Autoimmunerkrankungen auftreten. Mit Vitamin D und anderen Immunmodulatoren soll sich die Situation der Patienten in Zukunft grundlegend verbessern.
Die Funktion von Insulin
In Deutschland sind 300 000 bis 400 000 Menschen von Typ-1-Diabetes (T1D) betroffen und die Zahlen steigen jedes Jahr weiter an, sogar weltweit. T1D wird durch genetische Defekte oder eine Autoimmunerkrankung ausgelöst. Den Blutzuckerspiegel reguliert das Inselorgan in der Bauchspeicheldrüse, das aus circa einer Million Mikroorganen, den Langerhans-Inseln, besteht.
[dt_call_to_action content_size=”small” background=”fancy” line=”true” style=”1″]
[vc_toggle title=”Abkürzungen” style=”square” el_id=”1446040522748-fab84964-25f2″ css=”.vc_custom_1446052456701{margin-top: 15px !important;}”]
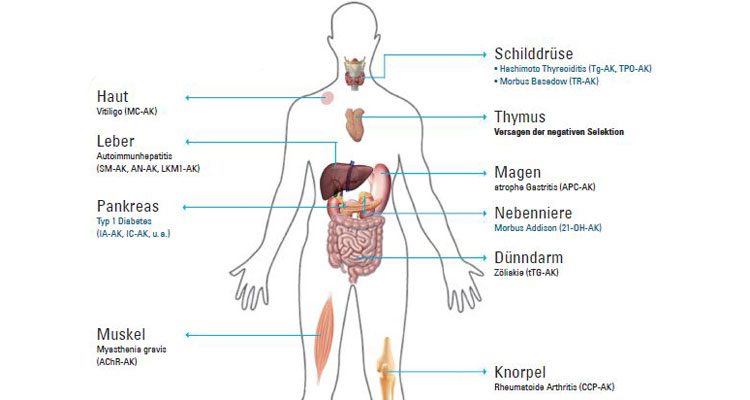
AK=Antikörper, Tg= Thyreoglobulin, TPO= Thyreoperoxidase, TR= Thyreotropin-Rezeptor, APC=Parietalzellen, 21-OH= 21-Hydroxylase, tTG=tissue-Transglutaminase, CCP=cyklische citrullinierte Peptide, AChR=Acetylcholin-Rezeptor, IA-AK= Insulinautoantikörper, IC= Inselzellen, IA2=Tyrosinphosphatase, GAD=Glutamatdecarboxylase, SM= smoothmuscel, AN= antinukleär, LKM1= Leber-Niere-Mikrosom 1, MC= Melanozyten
[/vc_toggle]
[/dt_call_to_action]
Diese Mikroorgane sind aus unterschiedlichen Zelltypen mit verschiedenen Aufgaben aufgebaut. So gibt es Zellen, die den Insulinspiegel im Blut messen und solche, die Insulin produzieren. Insulin regt die Körperzellen an, Glukose aufzunehmen, wodurch es zu einer Senkung des Blutzuckerspiegels kommt.
Entstehung und Folgen von Typ-1-Diabetes
T1D entsteht, wenn das Immunsystem isoliert die Insulin-produzierenden β-Zellen der Inselzellen zerstört. Es wird dann kein Insulin mehr produziert und der im Blut vorhandene Zucker kann nicht mehr in die Zellen aufgenommen werden. Ist der Blutzuckerspiegel auf Dauer erhöht, werden Diabeteskomplikationen begünstigt: Erkrankungen des Herz-Kreislauf-Systems, der Nieren, der Augen und der Nerven.

Dadurch verringert sich die Lebenserwartung von Patienten mit T1D im Durchschnitt um etwa zehn Jahre. Bis jetzt wird die Krankheit durch regelmäßiges Messen des Blutzuckers und feindosierte Insulingaben symptomatisch behandelt. Ein funktioneller Ausgleich kann durch Transplantation einer Bauchspeicheldrüse (zum Beispiel bei kombinierter Nieren- und Pankreastransplantation) erfolgen, jedoch reichen die Spenderorgane längst nicht aus.
Immunologische Grundlagen
Die Aufgabe des Immunsystems ist es, den Körper zu schützen. Es erkennt Krankheitserreger, Tumorzellen und Fremdkörper und macht sie unschädlich. Eigene Zellen werden anhand von Proteinen, die auf den Zelloberflächen lokalisiert sind, von fremden Zellen und Fremdkörpern unterschieden. Durch eine Reihe von Risikofaktoren kann dieses Erkennungssystem versagen und dann auch eigene Zellen angreifen. Die Folge sind Autoimmunkrankheiten, bei denen gezielt Organe oder wichtige Teile zerstört oder in ihrer Funktion gestört werden. Diese Erkrankungen können jeden und fast jedes Organ treffen.

Bei einigen Patienten richtet sich das Immunsystem gegen mehrere Organe. Bei dem autoimmunen polyglandulären Syndrom (APS) greift das Immunsystem sukzessive mehrere hormonbildende (endokrine) Organe und zum Teil weitere Gewebe an. Solche endokrinen Autoimmunerkrankungen sind unter anderem Typ-1-Diabetes, Hashimoto Thyreoditis, eine Schilddrüsenautoimmunerkrankung, und die Nebenniereninsuffizienz Morbus Addison. »Diese Kombination von Erkrankungen kann für die Betroffenen fatal sein, insbesondere bei Typ-1-Diabetes und Morbus Addison«, berichtet Prof. Klaus Badenhoop, Diabetologe an der Medizinischen Klinik I. Die Therapie der einzelnen Erkrankungen wird dadurch erschwert, dass es Wechselwirkungen mit der Behandlung der weiteren Krankheiten zu berücksichtigen gilt und schwer steuerbare Nebenwirkungen auftreten können.
Die ursächliche Behandlung des gestörten Immunsystems ist bisher nicht möglich, nur eine symptomatische Ersatztherapie der fehlenden Hormone. Eine komplette Unterdrückung des Immunsystems wie bei Organtransplantation oder systemischen Autoimmunerkrankungen kommt wegen der schweren Nebenwirkungen (Infektionen, Krebsrisiko) nicht infrage. Die lebenslang notwendige Hormonersatztherapie ist vordergründig einfach, aber im Alltag mit vielen Problemen sowie Risiken behaftet und schmälert darüber hinaus die Lebensqualität von Patienten und ihren Familien.
Risikofaktor Vitamin-D-Mangel
Risikofaktoren für Autoimmunerkrankungen sind eine genetische Veranlagung, vorangegangene Infektionen und ein Vitamin-D-Mangel. Dabei ist ein Vitamin-D-Mangel auch bei Gesunden weit verbreitet. Vorstufen des Vitamin D werden entweder durch Sonnenexposition in der Haut gebildet oder über die Nahrung aufgenommen, zum Beispiel durch Fisch oder mit Vitamin D angereicherte Nahrungsmittel. Der Körper stellt das Vitamin D bei ausreichender Versorgung mit den Vorstufen selbstständig her.

Bei geringer Versorgung mit Vorläufern resultiert ein Vitamin-D-Mangel. »Selbst im Sommer, wenn die meisten Menschen ihre Vitamin-D-Depots auffüllen, konnten wir zeigen, dass unabhängig von einer Autoimmunerkrankung ein beträchtlicher Anteil der Bevölkerung einen Vitamin-D-Mangel aufweist «, erklärt Prof. Badenhoop. Im Tiermodell und auch in menschlichen Zellsystemen hat Vitamin D einen positiven Effekt auf das Immunsystem und kann die zur Immunabwehr gehörenden T-Lymphozyten so umprogrammieren, dass sie toleranter gegenüber Zielantigenen werden.
»Dadurch besteht die Hoffnung, dass Patienten mit Autoimmunerkrankungen immunologisch stabilisiert und Nebenwirkungen einer Langzeittherapie mit Steroiden verringert werden können«, so Badenhoop. Die Arbeitsgruppe des Professors erforscht in einem Doktoranden-Projekt, gefördert von der Else Kröner-Fresenius-Stiftung, ob durch eine Therapie mit Vitamin D das autoimmun-aggressive Zellmilieu verbessert und letztlich die Zerstörung weiterer Organe vermieden werden kann. Es geht dabei um eine individualisierte Therapie mit höher dosiertem Vitamin D. Das Projekt hat sich über viele Jahre entwickelt und wird seit eineinhalb Jahren konkret umgesetzt.
»In einer Pilotstudie mit Patienten mit entweder Typ-1-Diabetes oder Morbus Addison konnten wir in einer Doppelblindstudie zeigen, dass das Immunsystem während der Einnahme von Vitamin D positiv beeinflusst wurde. Wurde kein Vitamin D mehr eingenommen, ging dieser Effekt verloren«, erklärt Badenhoop.
Die Immunstörung in weiteren Organen stoppen
Die beobachteten Effekte waren besonders deutlich, wenn der Ausgangsspiegel des Vitamin D der Probanden niedrig war bei Vorliegen bestimmter Genvarianten.

Solche pharmakogenetischen Einflussfaktoren erklären das unterschiedliche Ansprechen auf verschiedene Behandlungsarten. In der klinischen Routine ist ein Gentest nicht erforderlich.Hier soll die Vitamin-D-Dosis abhängig vom Ausgangswert festgelegt und durch Kontrollen des Vitamin-D Spiegels angepasst werden. Mit einer Kombination aus Vitamin D und einer modifizierten Glukokortikoid-Therapie, wie sie sich jetzt zum Beispiel schon in zugelassenen Präparaten für die Behandlung der Schuppenflechte bewährt hat, soll die Ausbreitung der Autoimmunerkrankung auf weitere Organe verhindert werden. Falls diese Konzepte erfolgreich sind, können auch noch gesunde Menschen mit stark erhöhtem Risiko für diese Erkrankungen frühzeitig behandelt und vor dem Vollbild der Krankheit geschützt werden.