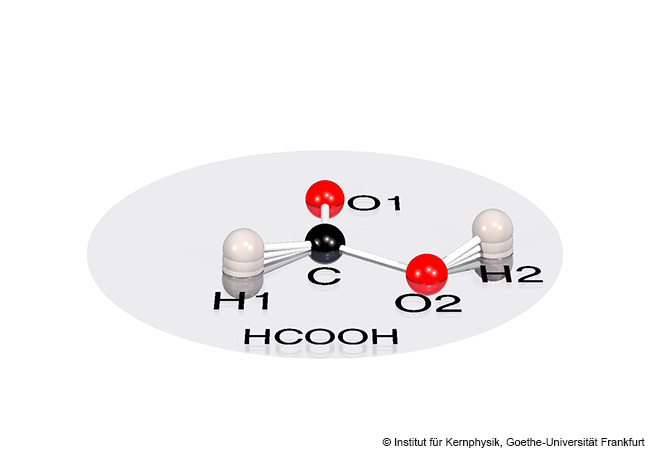
Ein Laserblitz von unvorstellbarer Intensität pulverisiert im Labor ein Molekül. Wachsam zeichnen die Instrumente die Flugbahn und Geschwindigkeit jedes Bruchstücks auf. Physiker gewinnen daraus hochpräzise Informationen über die Molekülstruktur. Auch links- und rechtshändige Formen lassen sich unterscheiden.
Welche Kräfte das Licht entwickeln kann, weiß jeder, der schon einmal beobachtet hat, wie ein Laserstrahl zentimeterdicke Metallplatten schneidet. Weiter steigern lässt sich die Spitzenleistung eines Lasers, wenn die Energie nicht mehr kontinuierlich, sondern in Pulsen abgegeben wird. In den letzten Jahrzehnten ist es gelungen, Laserpulse immer weiter zu verkürzen und damit die Spitzenintensität immer weiter zu erhöhen. Bei geeigneter Fokussierung kann selbst mit kommerziell erhältlichen Systemen für eine sehr kurze Zeit eine Intensität von 1016 Watt pro Quadratzentimeter erreicht werden. Dies entspricht der Sonneneinstrahlung, die auf ganz Europa fällt, fokussiert auf einen Stecknadelkopf.
Da sich Licht als elektromagnetische Welle beschreiben lässt, sind mit dieser Intensität unvorstellbar starke elektrische Felder verbunden, die enorme Kräfte auf geladene Teilchen wie beispielsweise Elektronen ausüben. Wenn ein Molekül in einen solchen Laserfokus gerät, sind die Kräfte auf die negativ geladenen Elektronen so groß, dass sie aus dem Molekül regelrecht herausgerissen werden. In der Folge explodiert das Molekül, bevor weitere Umordnungsprozesse stattfinden können.
Von der Explosion zur Strukturbestimmung
Warum führt man eine solche, in der Natur nicht vorkommende Situation herbei? Weil man nach der Molekülexplosion – Coulomb Explosion Imaging genannt – aus den Fragmenten etwas über die Struktur des Moleküls lernen kann: Gelingt es, die Flugrichtung und -geschwindigkeit der einzelnen Fragmente zu messen, lassen sich Rückschlüsse auf die ursprüngliche Anordnung im Molekül ziehen. Die Explosion fungiert gewissermaßen als Mikroskop, das die unvorstellbar kleine molekulare Welt in unseren Makrokosmos projiziert und somit messbar macht.
Die »Reaktionsmikroskope«, mit denen diese Messungen für Molekülfragmente möglich sind, wurden am Institut für Kernphysik der Goethe-Universität entwickelt und sind unter dem Namen COLTRIMS (Cold Target Recoil Ion Momentum Spectroscopy) mittlerweile in Laboren weltweit im Einsatz [1]. Im Gegensatz zu bekannteren Abbildungsmethoden mit atomarer Auflösung wie Rastertunnel- oder Rasterelektronenmikroskopen lassen sich hier individuelle Moleküle untersuchen, die in einem Molekülstrahl auftreten und nicht auf eine Trägersubstanz aufgebracht werden müssen. Nachdem viele Jahre nur sehr einfache Moleküle wie Stickstoff (N2) oder Wasser (H2O) untersucht werden konnten, ist die Technik mittlerweile auch auf komplexere Moleküle ausgedehnt worden.
[dt_call_to_action content_size=“small“ background=“fancy“ line=“true“ animation=“fadeIn“]
Auf den Punkt gebracht
- Sieben der zehn häufigsten Medikamente enthalten chirale Wirkstoffe – Moleküle, die in rechts- und linkshändiger Form auftreten können. Ihre Wirkung im Körper hängt entscheidend von der Händigkeit ab.
- Mit der Methode des Coulomb Explosion Imaging lässt sich die Händigkeit einzelner Moleküle bestimmen. Diese Methode ist hochpräzise, wurde aber bisher nur für einfache Strukturen erprobt.
[/dt_call_to_action]
Rechts- und linkshändige Moleküle unterscheiden
Eine interessante Anwendung, die kürzlich von unserer Arbeitsgruppe demonstriert wurde, besteht darin, chirale Moleküle zu unterscheiden und ihre mikroskopische Konfiguration zu bestimmen. In der Chemie wird ein Molekül als chiral bezeichnet, wenn es in zwei Formen vorkommt, deren geometrische Strukturen sich wie Bild und Spiegelbild verhalten. Der Prototyp für diese Art von Symmetrie sind unsere Hände – daher der Begriff »chiral«, der aus dem griechischen Wort für Hand abgeleitet ist.
Wenn zwei chirale Moleküle miteinander wechselwirken, spielt ihre jeweilige Händigkeit eine entscheidende Rolle – was sofort einleuchtet, wenn man sich als Analogie den Handschlag zweier Menschen zur Begrüßung vorstellt: Seinem Gesprächspartner spontan die linke Hand zu reichen, wird aller Voraussicht nach eine andere Reaktion hervorrufen, als die gewohnte rechte anzubieten.
Die Mehrzahl der biologisch relevanten Moleküle ist händig, beispielsweise viele Zucker und fast alle natürlich vorkommenden Aminosäuren. Auch unser Körper ist aus vielen chiralen Bausteinen aufgebaut. Somit reagieren Bild und Spiegelbild eines Moleküls unterschiedlich mit unserem Organismus – dies macht sich bei Geruchsstoffen, aber auch bei vielen Medikamenten bemerkbar. Sieben der zehn häufigsten Medikamente enthalten chirale Wirkstoffe; im Sinne der Arzneimittelsicherheit ist es deshalb wünschenswert, diese Wirkstoffe ausschließlich in der richtigen Händigkeit zu verabreichen. Die Unterscheidung der rechts- und linkshändigen Variante eines Moleküls ist daher von großem Interesse in der Pharmazie und in der Biochemie.
Methoden, um die beiden Händigkeiten durch Wechselwirkung mit polarisierter Strahlung oder durch eine Abfolge chemischer Reaktionen zu unterscheiden, gibt es zuhauf. Allerdings messen diese Techniken nur makroskopische Effekte, die von einer Vielzahl von Molekülen herrühren; die Bestimmung der mikroskopischen Anordnung der Atome im Molekül selbst (Absolutkonfiguration) ist meist nur indirekt möglich – entweder mithilfe aufwendiger Rechnungen oder durch chemische Reaktionen mit Stoffen bekannter Händigkeit. Zudem kann die Reinheit der Probe nur aus der Stärke des gemessenen Effekts bestimmt werden, für den wiederum eine Kalibrierung bei bekannter Konzentration notwendig ist.
Einzelne chirale Moleküle im Fokus
Für diese Probleme bietet das »Explosionsmikroskop « eine elegante Lösung. Wir konnten mit unserer Arbeit [2] zeigen, dass das einfachste chirale Molekül CHBrClF (Abb. 3) mithilfe der oben beschriebenen Laserpulse in seine fünf atomaren Bestandteile zerlegt werden kann. Diese fliegen in einer Explosion auseinander; die Impulse können mithilfe des COLTRIMS-Reaktionsmikroskops gemessen werden.
Da die Atome näherungsweise in Richtung der Bindungsachsen auseinanderfliegen, lässt sich aus diesen Impulsen für jedes Molekül eindeutig bestimmen, ob es sich um die rechts- oder linkshändige Variante handelt. Damit eröffnet sich die Möglichkeit, die Konfiguration exakt zu bestimmen. Auch zur Analyseder Reinheit ist diese Methode geeignet: Da die Händigkeit für einzelne Moleküle gemessen wird, muss nur die Anzahl der rechts- und linkshändigen Moleküle verglichen werden, um eine zuverlässige Aussage über den jeweiligen Anteil zu erhalten.
Entscheidend im Hinblick auf eine zukünftige Anwendung als Analysemethode ist die Frage, inwieweit sich die Explosion und die Messung der Fragmente auf komplexere Moleküle ausdehnen lassen. Hierzu haben wir bereits erste Experimente an größeren Molekülen durchgeführt, die eine Bestimmung der Absolutkonfiguration aussichtsreich erscheinen lassen.
Die mit diesen Arbeiten gewonnenen Erkenntnisse sind nicht nur für zukünftige Anwendungen, sondern auch für die Grundlagenforschung von Relevanz: Die Analyse der Fragmentationsprozesse ermöglicht ein besseres Verständnis der Unterschiede zwischen rechts- und linkshändigen Molekülen auf quantenphysikalischer Ebene. Die Untersuchung
einzelner chiraler Moleküle könnte somit zu einem Werkzeug werden, um fundamentale Symmetrieeigenschaften der physikalischen Gesetze zu untersuchen, die die Welt der Moleküle und damit viele lebenswichtige Prozesse beschreiben.
[dt_call_to_action content_size=“small“ background=“fancy“ line=“true“ animation=“fadeIn“]
Die Autoren

Dr. Markus Schöffler, Jahrgang 1978, studierte Physik an der Goethe-Universität. Mit einem Feodor-Lynen-Stipendium der Humboldt-Stiftung ging er zuerst an die Advanced Light Source in Berkeley und für ein weiteres Postdoktorat an die Technische Universität Wien. Ende 2011 kehrte er zurück nach Frankfurt und widmet sich seither vor allem der Erforschung chiraler Systeme mithilfe von Reaktionsmikroskopen. Seine Arbeiten wurden 2014 mit dem Adolf-Messer-Stiftungspreis ausgezeichnet.
schoeffler@atom.uni-frankfurt.de
Prof. Dr. Reinhard Dörner, Jahrgang 1961, studierte Physik an der Goethe-Universität, wo er sich nach der Promotion (1991) habilitierte (1998). Forschungsaufenthalte führten ihn an das Lawrence Berkeley National Laboratory in den USA. 2002 wurde er auf eine Professur für Experimentalphysik an der Goethe-Universität berufen. Seine Arbeit wurde als eines der renommierten Kosseleck-Projekte der Deutschen Forschungsgemeinschaft gefördert. 2015 erhielt er den Robert-Wichard-Pohl-Preis der Deutschen Physikalischen Gesellschaft für interdisziplinäre Beiträge zur Physik. Sein Interesse gilt auch der Verbindung von Physik und Philosophie. doerner@atom.uni-frankfurt.de
Dr. Martin Pitzer, Jahrgang 1984, studierte Physik am Karlsruher Institut für Technologie und an der Ecole Polytechnique Fédérale Lausanne. Seine Dissertation zum Thema »Koinzidenzmessungen an chiralen Molekülen« fertigte er an der Goethe-Universität in der Gruppe von Reinhard Dörner an. In Zukunft wird er seine Forschung im Rahmen einer eigenständigen Nachwuchsstelle an der Universität Kassel weiterführen. pitzer@atom.uni-frankfurt.de
[/dt_call_to_action]
Der Beitrag ist erschienen in Forschung Frankfurt 2/2015. Wenn Licht Moleküle in Stücke reißt